��Ŀ����
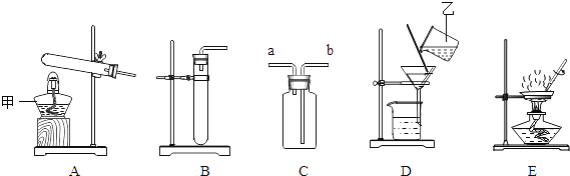
����Ŀ��Ϊ̽�������Թ�������(H2O2)�ֽ�Ĵ�Ч����ij�о�С��������ͼ��ʾ��ʵ�顣
ʵ��һ��
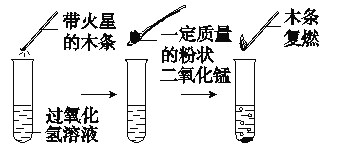
ʵ��������ݼ�¼��
1%����������Һ/mL | 50 | 50 | 50 |
����������̵�����/g | 0.1 | 0.2 | 0.4 |
����40 sĩ�õ����������/mL |
ʵ��һ��ͼ�е�ʵ���ܷ�֤�����������ǹ�������ֽⷴӦ�Ĵ�������˵�����ɣ�__________��
ʵ������ӱ������ƿ��Կ�������ʵ���Ŀ����____________��
���𰸡�����֤�����ڹ���������Һ�м���������̺�ӿ��˷�Ӧ���ʣ���û��֤�����������ڷ�Ӧǰ��������ͻ�ѧ���ʲ���̽�������������뻯ѧ��Ӧ���ʵĹ�ϵ
��������
���ݶԱ�ʵ��������
ʵ��һ��ͼ�е�ʵ�鲻��֤�����������ǹ�������ֽⷴӦ�Ĵ������ڹ���������Һ�м���������̺�ӿ��˷�Ӧ���ʣ���û��֤�����������ڷ�Ӧǰ��������ͻ�ѧ���ʲ�����ʵ������ӱ������ƿ��Կ������ı���Ǽ���������̵��������ʸ�ʵ���Ŀ����̽�������������뻯ѧ��Ӧ���ʵĹ�ϵ��

����Ŀ������һС����ɫ���壬���к��������ƺ��������Ȼ��ơ������ơ�Ϊ�˳�ȥ�Ȼ��ơ������ƣ��õ������������ƹ��壬ͬѧ�ǽ�������ʵ�顣
ʵ�鲽�� | ʵ����� |
�ܽ� | ����ɫ��������ձ��У�����������ˮ���ò��������裬�õ�����������ҺA����������������________�� |
���� | ��һ��������ҺA�м����������������Һ��������ɫ������д��������Ӧ�Ļ�ѧ����ʽ________�� �����������������Һ��Ŀ����_ �ڶ�������ַ�Ӧ���������м��������________��Һ���۲쵽��ɫ�������ࡣ ������������������ᄇ��һ��ʱ�����________����������ƣ����õ��������ҺB�Ͱ�ɫ��������ҺB�е�������________�� |
���� | ����ҺB�м��������ϡ���ᣬ��ַ�Ӧ��Һ�嵹���������У����������г���________ʱ��ֹͣ���ȣ����ɵõ������������ƾ��塣 |
����˼���й����ʳ��ӵ����⣬����Ҫѡ����ȷ���Լ�����Ҫע�������Լ���˳���������Ӳ����е�һ���͵�: ����˳��ߵ��������________��