题目内容
【题目】小冰将215.2g硝酸银溶液倒入一定量铜粉中,充分反应后,过滤,得到200g只含一种溶质的滤液和43.2g固体,所得滤液中含溶质的质量分数是( )
A. 6.6% B. 9.4% C. 18.8% D. 22.3%
【答案】B
【解析】
解法一:设反应生成硝酸铜的质量为x,
铜粉的质量为:200g+43.2g-215.2g=28g,
Cu+2AgNO3=Cu(NO3)2+2Ag,溶液质量差
340 188 340-188=152
x 215.2g-200g=15.2g
![]()
x=18.8g,
所得滤液中含溶质的质量分数是:![]() ×100%=9.4%。故选:B。
×100%=9.4%。故选:B。
解法二:设反应生成硝酸铜的质量为x,
铜粉的质量为:200g+43.2g-215.2g=28g,
Cu+2AgNO3=Cu(NO3)2+2Ag,
64 188 216
![]() x
x ![]()
根据题意有:28g-![]() +
+![]() =43.2g,
=43.2g,
x=18.8g,
所得滤液中含溶质的质量分数是:![]() ×100%=9.4%。故选:B。
×100%=9.4%。故选:B。

练习册系列答案
相关题目
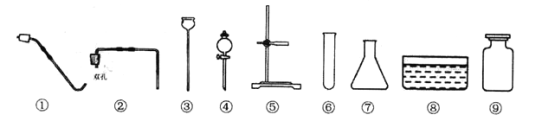
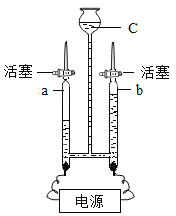
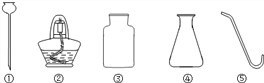
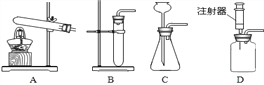
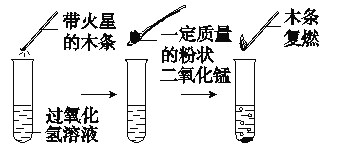
【题目】为探究催化剂对过氧化氢(H2O2)分解的催化效果,某研究小组做了如图所示的实验。
实验一:
实验二:数据记录表
1%过氧化氢溶液/mL | 50 | 50 | 50 |
加入二氧化锰的质量/g | 0.1 | 0.2 | 0.4 |
测量40 s末得到氧气的体积/mL |
实验一:图中的实验能否证明二氧化锰是过氧化氢分解反应的催化剂?并说明理由:__________。
实验二:从表格的设计可以看出,该实验的目的是____________。