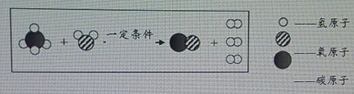
题目内容
【题目】某同学利用石灰石和稀盐酸进行如下实验,操作过程和数据如图(样品中杂质不与酸反应也不溶于水)。
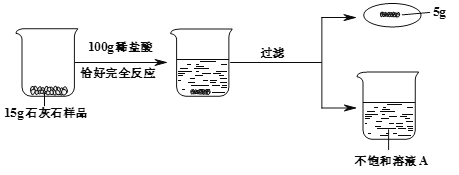
(1)15g石灰石样品中CaCO3物质的量。
(2)列式计算不饱和溶液A的溶质质量分数(结果准确到0.1%)。
【答案】(1)0.1mol ; (2) 10.0%
【解析】(1)根据碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,样品中的杂质不与酸反应也不溶于酸,所以恰好反应后剩余的固体为杂质,15g石灰石样品中CaCO3的质量为15g5g=10g,n=![]() ; (2)设生成氯化钙的质量为
; (2)设生成氯化钙的质量为![]() ,生成二氧化碳的质量为y
,生成二氧化碳的质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
10g ![]() y
y
![]()
![]() =11.1g,
=11.1g, ![]() =4.4g
=4.4g
不饱和溶液A的溶质质量分数![]() 。
。
答:不饱和溶液A的溶质质量分数为10.0% 。

 步步高达标卷系列答案
步步高达标卷系列答案【题目】(1)下表是CO2气体在水中的几组溶解度数据(单位:mL/100mL水)
溶解度 温度(℃) 大气压 | 0 | 25 | 50 | 75 | 100 |
1 | 1.79 | 0.752 | 0.423 | 0.307 | 0.231 |
10 | 15.92 | 7.14 | 4.095 | 2.99 | 2.28 |
25 | 29.30 | 16.20 | 9.71 | 6.82 | 5.73 |
①根据CO2的溶解度表,可以得出气体的溶解度随外界条件的变化规律是:__________、____。
②打开可乐瓶有气体逸出,说明原瓶中的压强_________(填“>”、“<”或“=”)瓶外大气压强。
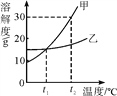
(2)甲、乙两物质(均不含结晶水)的溶解度曲线如下图,请回答

① t2℃时,甲、乙两物质溶解度较大的是___________。
② t1℃时,50g水中加入30g乙,充分溶解所得溶液的质量是___________g。
③ t2℃时,将乙的不饱和溶液转化为饱和溶液一定可行的方法 是___________(填编号)。
A.加足量溶质乙 B.蒸发溶剂至晶体析出 C.降温
④ t2℃时,甲、乙溶液的溶质质量分数相等且均为a%,则甲溶液一定为__________(填“饱和”或“不饱和”)溶液,a%的取值范围为___________。
⑤ 将t2℃等质量的甲、乙饱和溶液分别降温到t1℃,有关说法正确的是___________。
A.t1℃时溶质质量:甲=乙 B.t1℃时溶剂质量:甲>乙
C.t1℃时溶液质量:甲<乙 D.析出晶体质量:甲>乙