题目内容
【题目】某同学欲配制一定溶质质量分数的NaCl溶液,他准备了下列实验仪器。
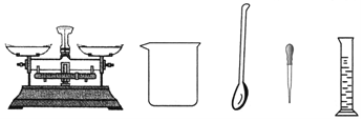
请填空:
⑴配制时可按下列实验步骤进行:计算→称量→_______→溶解。
⑵称量时,NaCl固体粉末应放在托盘天平_________(填“左盘”或“右盘”)的纸片上。
⑶配制过程中为促进NaCl的溶解,还需要的一种玻璃仪器是_______(填仪器名称)。
⑷量取一定体积的水,除了用量筒外,还需要用____________(填仪器名称)。
【答案】 量取 左盘 玻璃棒 胶头滴管
【解析】本题考查了配制一定质量的溶质质量分数的溶液。
(1)配制时可按下列实验步骤进行:计算→称量→量取→溶解;
(2)称量时,药瓶不能直接放在托盘上,可放在称量纸上,且左物右码;
(3)配制过程中为促进NaCl的溶解,还需要的一种玻璃仪器是玻璃棒;
(4)用量筒量取一定的体积液体时,应选择合适的量筒;向量筒内加液时,先用倾倒法加液到近刻度线,再改用胶头滴管加液到刻度线,除了用量筒外,还需要用胶头滴管。

【题目】如下图所示,把足量的硫粉放入氧气中充分燃烧。
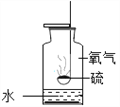
(1)硫在氧气中燃烧的反应方程式是______________________________。
(2)实验后,取少量集气瓶内的溶液于试管中,再往试管中滴加数滴的紫色
石蕊溶液,振荡。发现紫色石蕊溶液变成红色。
(提示:石蕊溶液是将石蕊加入水中溶解后得到的混合物)
【提出问题】是什么物质使紫色石蕊变红色呢?
【提出假设】假设1:水使紫色石蕊变红;
假设2:________________________使紫色石蕊变红;
假设3:二氧化硫与水反应的生成物使紫色石蕊变红。
【设计实验】
① 我们可判断假设____________不成立,因为石蕊溶液中含有这种物质,不能使紫色变红。
② 请设计一个实验方案验证另外两个假设是否成立,用文字描述实验步骤及填写预期实验现象和结论。(提供的试剂和用品有:干燥的紫色石蕊纸花若干朵、干燥的二氧化硫两瓶、水)
实验步骤 | 预期实验现象和结论 |
___________________________ | __________________________, 假设___________不成立。 |
____________________________ | __________________, 假设____________成立。 |
【题目】甲烷(化学式为CH4)不完全燃烧时生成水和其它氧化物。某实验小组对此展开研究:
①常用___________检验生成物中是否含有水②对燃烧产物中的其它氧化物进行探究:(图中固定试管的仪器已略去)
假设 | 实验 | 现象 | 结论 |
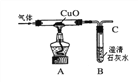
生成物中有一氧化碳 | 用下图装置进行实验
| A中的现象是 ________ | 生成物中含有一氧化碳。写出A中的反应化学方程式是______ |
进一步查阅资料,发现CO能溶于铜液(醋酸二氨合铜和氨水的混合液)。因此可在装置B后再连接下图装置D,其目的是______,装置B、D的连接顺序:导管C连接____(填“E”或“F”)。

实验小组通过装置B中石灰水变浑浊判断燃烧产物中一定含有二氧化碳,你觉得该实验小组的判断是否正确?若不正确,请设计简单实验判断燃烧产物中是否含有二氧化碳______。
【题目】同学们可以通过下列方式认识空气。
【组成角度】
①空气中体积分数约为78%的物质是___________。
②为测定空气中氧气体积分数,设计下图实验。
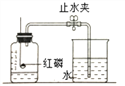
Ⅰ.为了确保实验成功,在装药品之前应该检查装置的 _________;
Ⅱ.该实验中红磷需要过量的原因是__________;
Ⅲ.红磷燃烧的现象是____________,反应的化学方程式 ____________;
Ⅳ.冷却至室温后打开止水夹观察到的现象是 _______________;由此得出空气中氧气的体积分数约为 ___________。
【微观角度 】
①用“化学符号”或“图示”填空。
![]()
图 示 |
| ______ |
|
化学符号 | ______ | N2 | _______ |
②同温同压下,气体的体积比等于分子个数比。若忽略空气中其它成分,如图可表示空气微观模型的是__________(填选项)。
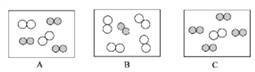
【变化角度】
在一个标准大气压下,空气中部分组分的沸点如下:
组分 | 氮气 | 氧气 | 二氧化碳 |
沸点(℃) | -195.8 | -183.0 | -78.4 |
①将燃着的木条置于盛有表中组分的混合液的钢瓶口,观察到的现象是____________。
②下列叙述错误的是_____________。
A.木炭在氧气中燃烧,发出白光
B.铁丝在空气中燃烧,火星四射,生成黑色固体
C.从冰箱里拿出汽水,瓶子外表有液珠,说明空气中有水蒸气
D.久置澄清石灰水的试剂瓶内壁有一层白膜,证明空气中有二氧化碳
③铁丝在氧气中燃烧的化学方程式是____________。
【应用角度】
①酒精(C2H5OH)是一种常用消毒剂,酒精由___________种元素组成,其中氢元素与氧元素的质量比为_______;氢元素的质量分数为________(可用分数表示);每个酒精分子含________个原子;46gC2H5OH中含_________个氧原子。配平酒精燃烧的化学方程式的系数依次为_______。
□C2H5OH+□O2![]() □CO2+□H2O
□CO2+□H2O
②食品包装内充N2以防腐,因为N2的化学性质_____________;