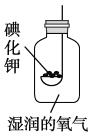
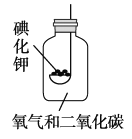
题目内容
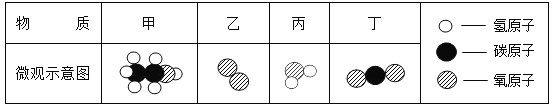
【题目】在一个密闭容器中,有甲、乙、丙、丁四种物质在一定条件下充分反应后,测得反应前后各物质的质量如下表:下列说法错误的是( )
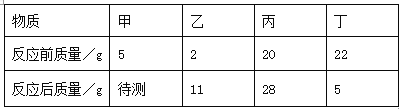
A. 该反应是分解反应 B. 甲可能是该反应的催化剂
C. 乙、丙变化的质量比为9:8 D. 反应后甲的质量为0
【答案】D
【解析】反应后质量增加的物质是生成物,反应后质量减少的物质是反应物,反应前后质量不变的物质可能是催化剂,据此结合质量守恒定律分析解答即可。根据质量守恒定律,可知物质甲反应后的质量为:x=2g+5g+20g+22g-11g-28g-5g=5g,故甲可能是该反应的催化剂,B正确,D错误;乙的质量增加,为生成物;丙的质量增加,为生成物;丁的质量减少,为反应物,故该反应是甲生成乙和丙,为分解反应,A正确;C. 乙的质量增加9g、丙增加8g, 乙、丙变化的质量比为9:8,正确;故选D。

 全能练考卷系列答案
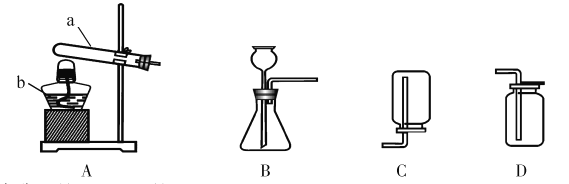
全能练考卷系列答案【题目】如下图所示,把足量的硫粉放入氧气中充分燃烧。
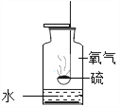
(1)硫在氧气中燃烧的反应方程式是______________________________。
(2)实验后,取少量集气瓶内的溶液于试管中,再往试管中滴加数滴的紫色
石蕊溶液,振荡。发现紫色石蕊溶液变成红色。
(提示:石蕊溶液是将石蕊加入水中溶解后得到的混合物)
【提出问题】是什么物质使紫色石蕊变红色呢?
【提出假设】假设1:水使紫色石蕊变红;
假设2:________________________使紫色石蕊变红;
假设3:二氧化硫与水反应的生成物使紫色石蕊变红。
【设计实验】
① 我们可判断假设____________不成立,因为石蕊溶液中含有这种物质,不能使紫色变红。
② 请设计一个实验方案验证另外两个假设是否成立,用文字描述实验步骤及填写预期实验现象和结论。(提供的试剂和用品有:干燥的紫色石蕊纸花若干朵、干燥的二氧化硫两瓶、水)
实验步骤 | 预期实验现象和结论 |
___________________________ | __________________________, 假设___________不成立。 |
____________________________ | __________________, 假设____________成立。 |