题目内容
【题目】根据所学知识并结合下列仪器,回答有关问题:
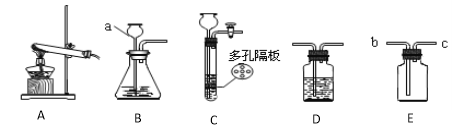
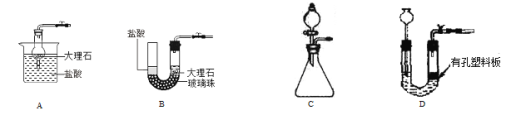
(1)写出图中标有字母的仪器的名称:a__________。
(2)实验室用A装置制取氧气,反应的化学方程式为 ;如要制取并收集二氧化碳,可选用的装置组合是 ,反应的化学方程式是 ,用D装置来检验二氧化碳,装置内发生的化学方程式是 。
(3)实验室制取氢气的化学方程式是 ,如果用如图放置的E装置收集该气体,则气体从___________端进入(填“b”或“c”);实验室常用装置C代替装置B制取氢气,该装置的优点是通过开关活塞来控制反应的开始和停止,下图和此装置原理相同的是 。
(4)在分子运动实验中,为帮助同学解决认识中的误区,爱实验的小赵改进了实验装置,如左图所示:实验过程中能观察到A试管中的实验现象是 ,约4分钟后才会观察到B中现象,为能快速观察B中的现象,同学们提出用热毛巾捂住B试管,依据是 。

【答案】(1)长颈漏斗。
(2) 2KClO3![]() 2KCl+3O2↑ BE或CE,CaCO3+2HCl=CaCl2+H2O+CO2↑ CO2+Ca(OH)2=CaCO3↓+H2O
2KCl+3O2↑ BE或CE,CaCO3+2HCl=CaCl2+H2O+CO2↑ CO2+Ca(OH)2=CaCO3↓+H2O
(3)Zn+H2SO4= Zn SO4 + H2↑,c,ABD。
(4)棉花上的酚酞很快变红了,温度升高,分子的运动速率变快
【解析】
试题分析:(1)图中标有字母a的仪器的名称是长颈漏斗 (2)A装置适用于给固体加热制取气体,试管口没有放棉花团,故是用氯酸钾制取氧气,2KClO3 ![]() 2KCl+3O2↑,制取二氧化碳是固液反应,常温进行,它易溶解于水,密度比空气大只能用向上排空气法收集,故选BE或CE,制取二氧化碳的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑ 检验二氧化碳用澄清石灰水,化学方程式是:CO2+Ca(OH)2=CaCO3↓+H2O(3)实验室用锌与稀硫酸反应制取氢气,Zn+H2SO4= ZnSO4 + H2↑,氢气的密度比空气小,进入E装置后容易占据上方空间,空气则被排到下方,易从b端排出,故c端是进气口。C装置的原理是关闭活塞,试管内压强增大,液体被压入长颈漏斗,使得固液不再接触,从而控制反应的进行,与此装置原理相同的是A、B、D装置 (4)浓氨水具有挥发性,挥发出的氨分子能使酚酞试液变红,温度越高,分子运动速度越快
2KCl+3O2↑,制取二氧化碳是固液反应,常温进行,它易溶解于水,密度比空气大只能用向上排空气法收集,故选BE或CE,制取二氧化碳的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑ 检验二氧化碳用澄清石灰水,化学方程式是:CO2+Ca(OH)2=CaCO3↓+H2O(3)实验室用锌与稀硫酸反应制取氢气,Zn+H2SO4= ZnSO4 + H2↑,氢气的密度比空气小,进入E装置后容易占据上方空间,空气则被排到下方,易从b端排出,故c端是进气口。C装置的原理是关闭活塞,试管内压强增大,液体被压入长颈漏斗,使得固液不再接触,从而控制反应的进行,与此装置原理相同的是A、B、D装置 (4)浓氨水具有挥发性,挥发出的氨分子能使酚酞试液变红,温度越高,分子运动速度越快

【题目】我国青海湖采集的天然碱样品可表示为aNa2CO3·bNaHCO3·cH2O(a、b、c为最简整数比)。小红同学为测定其组成,称取该天然碱样品16.6g进行如下实验:
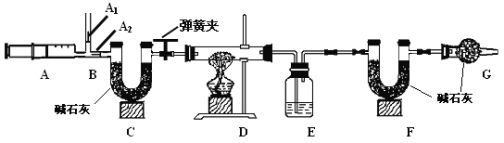
已知:1.碳酸钠比较稳定,加热不分解;
2. 2NaHCO3![]() Na2CO3 +CO2 ↑+H2O
Na2CO3 +CO2 ↑+H2O
3.图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,
A1打开进空气,A2关闭。
(一)实验步骤
(1)实验时,组装好装置,实验前应先 ,后续实验步骤是:
① 反复推拉注射器
② 称量E、F的质量
③ 关闭弹簧夹,加热D处试管直到反应不再进行
④ 打开弹簧夹,再次反复缓缓推拉注射器
⑤ 再次称量E、F的质量。
(二)问题探究:
(2) E中的药品为 ,E的作用是 。实验过程中,C的作用是 , F的作用是 。写出 F装置中所发生反应的一个化学方程式 。
(3)实验步骤②与③能否颠倒 (填“能”或“不能”)。若不进行步④的操作,则所测得的碳酸氢钠质量 (填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是 ;若没有G装置,则碳酸氢钠的质量 (填“偏大”、“偏小”、“无影响”)。
(4)下表是实验记录数据:
反应前 | 反应后 |
E的质量为100.0g | E的质量为102.25g |
F的质量为50.0g | F的质量为51.1g |
则: ① 碳酸氢钠分解生成二氧化碳的质量为 g
② 碳酸氢钠的质量为 g
③ 该天然碱的化学式中a:b:c= 。