题目内容
【题目】将一定质量的金属锌投入63.7g稀硫酸中,恰好完全反应,放出气体的质量与反应时间的关系如图所示.试求(计算结果精确到0.1%):

(1)完全反应后生成氢气的质量为 g
(2)所用硫酸溶液中溶质的质量分数(写出计算过程)
(3)反应结束后所得溶液的质量。
【答案】(1)0.2g;(2)所用硫酸溶液中溶质的质量分数是15.4%;(3)反应结束后所得溶液的质量是70g.
【解析】
试题分析:(1)由放出气体的质量与反应时间的关系图可知,生成氢气的质量为0.2g;
(2)设参加反应锌、硫酸溶液中溶质的质量分别为x、y
Zn + H2SO 4=ZnSO4 + H 2↑
65 98 2
x y 0.2g
![]()
解得:x=6.5g y=9.8g
所用硫酸溶液中溶质的质量分数为: ![]() ×100%=15.4%
×100%=15.4%
(3)由质量守恒定律可知,反应结束后所得溶液的质量为:63.7g+6.5g﹣0.2g=70g.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某实验小组的同学用碳酸钠粉末、粒状大理石、稀盐酸、浓盐酸、稀硫酸这几种
药品,探究哪两种药品的反应适合在实验室制取CO2。请你参与探究并回答问题。
【提出问题】上述酸和碳酸盐的反应是否适合在实验室制取CO2?
【方案设计】大家经过讨论,一致认为浓盐酸不适合用于实验室制取CO2,你认为原因
是 。
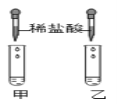
讨论后大家设计了如下三个实验进行对比分析。
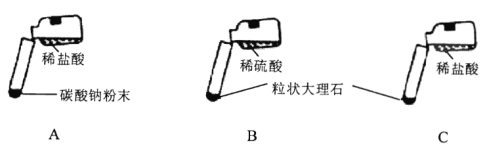
【实验与结论】(1)请你填写实验报告中①、②处的内容。
实验 | 实验现象 | 实验结论 |
A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,气体不便收集,不宜于实验室制取二氧化碳 |
B | 产生气泡,速率迅速减慢,反应几乎停止。 | 无法持续产生CO2,不能用于实验室制取CO2 |
C | ① | ② |
(2)根据探究结论,实验室制取二氧化碳所发生反应的化学方程式为 。
【拓展与迁移】(1)由上述探究可知,在确定实验室制取气体的反应原理时,要考虑诸多因素,例如反应速率要适中,便于收集等。请你再写出一种需要考虑的因素: 。
(2)实验室制取二氧化碳,为了控制反应速率,可以采用哪种方式向反应容器中加入酸? 。
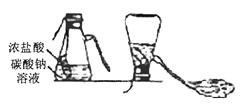
(3)如图是一种灭火器的工作原理示意图,其中用碳酸钠和浓盐酸反应来产生CO2的理由是 。