题目内容
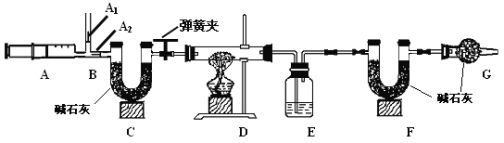
【题目】我国青海湖采集的天然碱样品可表示为aNa2CO3·bNaHCO3·cH2O(a、b、c为最简整数比)。小红同学为测定其组成,称取该天然碱样品16.6g进行如下实验:
已知:1.碳酸钠比较稳定,加热不分解;
2. 2NaHCO3![]() Na2CO3 +CO2 ↑+H2O
Na2CO3 +CO2 ↑+H2O
3.图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,
A1打开进空气,A2关闭。
(一)实验步骤
(1)实验时,组装好装置,实验前应先 ,后续实验步骤是:
① 反复推拉注射器
② 称量E、F的质量
③ 关闭弹簧夹,加热D处试管直到反应不再进行
④ 打开弹簧夹,再次反复缓缓推拉注射器
⑤ 再次称量E、F的质量。
(二)问题探究:
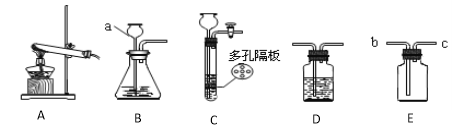
(2) E中的药品为 ,E的作用是 。实验过程中,C的作用是 , F的作用是 。写出 F装置中所发生反应的一个化学方程式 。
(3)实验步骤②与③能否颠倒 (填“能”或“不能”)。若不进行步④的操作,则所测得的碳酸氢钠质量 (填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是 ;若没有G装置,则碳酸氢钠的质量 (填“偏大”、“偏小”、“无影响”)。
(4)下表是实验记录数据:
反应前 | 反应后 |
E的质量为100.0g | E的质量为102.25g |
F的质量为50.0g | F的质量为51.1g |
则: ① 碳酸氢钠分解生成二氧化碳的质量为 g
② 碳酸氢钠的质量为 g
③ 该天然碱的化学式中a:b:c= 。
【答案】(1)实验前应先 检查装置的气密性
(2) E中的药品为 浓硫酸 ,E的作用是 吸水 C的作用是 吸收空气中的CO2和H2O F的作用是 吸收生成的二氧化碳 F装置中所发生反应的一个化学方程式 CO2+2NaOH==Na2CO3+H2O
(3) 不能 (填“能”或“不能”) 偏小 (填“偏大”、“偏小”、“无影响”)
推注射器时缓缓的目的是 防止气体流速太快,来不及被吸收
碳酸氢钠的质量 偏大 (填“偏大”、“偏小”、“无影响”)。
① 碳酸氢钠分解生成二氧化碳的质量为 1.1 g
② 碳酸氢钠的质量为 4.2 g
③ 该天然碱的化学式中a:b:c= 2:1:2 。
【解析】
试题分析∶这是一道综合题,通过实验探究和计算解决有关问题。检查装置的气密性是实验前首要操作。E中的药品为 浓硫酸 ,作用是 吸水 C中碱石灰作用是 吸收空气中的CO2和H2O 。 F中碱石灰作用是 吸收生成的二氧化碳,其反应的化学方程式是CO2+2NaOH==Na2CO3+H2O 。⑶关于误差的分析,④ 打开弹簧夹,再次反复缓缓推拉注射器是为了使产生的二氧化碳和水蒸气全部被吸收,否则所测得的碳酸氢钠质量会偏小。若没有G装置,空气中二氧化碳会被F装置吸收,这样碳酸氢钠的质量会偏大。(4)根据化学方程式和题中相关信息计算。
考点∶考查综合分析问题和解决问题的能力。

 53随堂测系列答案
53随堂测系列答案