题目内容
【题目】如图中A、B、C、D、E、F为初中化学常见的六种物质。D、E、F均含有一种相同的元素,D是一种黑色粉末,F的溶液为蓝色,A与B均可用于金属除锈,C和F属于同一类别的物质(图中“![]() ”表示两种物质能发生反应,用“
”表示两种物质能发生反应,用“![]() ”或“
”或“![]() ”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。请回答下列问题:
”表示两种物质间能单向或双向转化,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行,物质是溶液的只考虑溶质)。请回答下列问题:
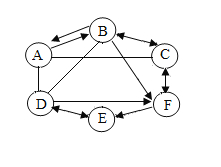
(1)分别写出A、B、E、F四种物质的化学式。
A:______B:______E:______F:______。
(2)D与足量A溶液反应的现象是______。
(3)F转化成C的化学方程式为______。
【答案】![]() HCl Cu
HCl Cu ![]() 固体溶解,溶液由无色变蓝色
固体溶解,溶液由无色变蓝色 ![]()
【解析】
D、E、F均含有一种相同的元素,F的溶液为蓝色,故F中含有铜离子,假设F为氯化铜;D是一种黑色粉末,D可能为氧化铜;E中含有铜元素可能为铜单质;A与B均可用于金属除锈,故可能均为酸,为硫酸、盐酸;C和F属于同一类物质,为盐;D(氧化铜)和E(铜)可以相互转化:氧化铜和氢气在加热条件下反应生成铜和水,加热条件下铜和氧气反应生成氧化铜;D(氧化铜)反应生成F,D(氧化铜)与B(盐酸)能反应,B(盐酸)反应生成F(氯化铜),均指:氧化铜和盐酸反应生成氯化铜和水; F(氯化铜)反应生成E(铜):氯化铜和铁反应生成氯化亚铁和铜;A(硫酸)反应生成C(盐酸):稀硫酸和氯化钡反应生成硫酸钡沉淀和盐酸,B(稀盐酸)和D氧化铜反应生成氯化铜和水;氯化铜F和氢氧化钡反应生成氯化钡C和氢氧化铜沉淀,氯化钡C和硫酸铜反应生成硫酸钡沉淀和氯化铜F,B盐酸和氢氧化钡反应生成氯化钡C和水,代入图示推导正确。因此![]() 分别是硫酸、盐酸、氯化钡、氧化铜、铜、氯化铜。
分别是硫酸、盐酸、氯化钡、氧化铜、铜、氯化铜。
(1)A、B、E、F四种物质分别是硫酸、盐酸、铜、氯化铜,化学式分别是![]() 、HCl、Cu、
、HCl、Cu、![]() 。
。
(2)D(氧化铜![]() 与足量A(硫酸
与足量A(硫酸![]() 溶液反应生成硫酸铜和水,现象是固体溶解,溶液由无色变蓝色。
溶液反应生成硫酸铜和水,现象是固体溶解,溶液由无色变蓝色。
(3)F(氯化铜![]() 转化成
转化成![]() 氯化钡
氯化钡![]() 的化学方程式为:
的化学方程式为:![]() 。
。

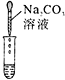
【题目】除去下列物质中的少量杂质,所用试剂和操作方法都正确的是
选项 | 物质 | 杂质 | 试剂 | 操作方法 |
A | 氧化钙 | 碳酸钙 | 无 | 高温煅烧 |
B | Ag | Fe | 足量的 | 充分反应后过滤 |
C |
| 水蒸气 | 足量生石灰 | 通过盛生石灰的干燥管 |
D |
| KCl | 适量 | 过滤 |
A.AB.BC.CD.D
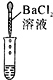
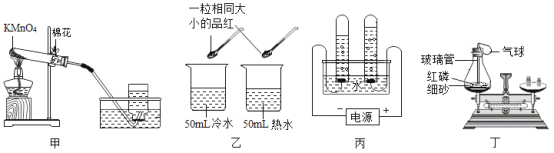
【题目】如图所示,在乙瓶中放入用石蕊溶液染成紫色的干燥的纸花,在 A 处缓缓地持续通入混合气体 X,下表中的物质及实验操作后的现象对应关系不正确的是
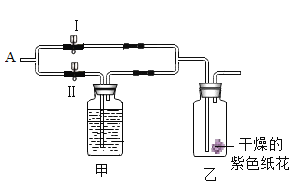
选项 | 气体 X | 甲中盛放的溶液(足量) | 关闭Ⅰ阀打开Ⅱ阀 |
A | 潮湿的混有一氧化碳的二氧化碳 | 浓硫酸 | 纸花不变色 |
B | 干燥的混有一氧化碳的二氧化碳 | 氢氧化钠溶液 | 纸花变为红色 |
C | 潮湿且混有氯化氢的二氧化碳 | 氢氧化钠溶液 | 纸花不变色 |
D | 干燥且混有氯化氢的二氧化碳 | 饱和碳酸氢钠溶液 | 纸花变为红色 |
A.AB.BC.CD.D
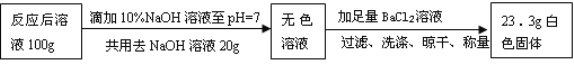
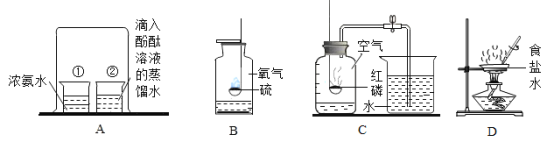
【题目】U形管在实验中有广泛的应用。
实验一:探究分子的性质 | 实验二:验证氧化钙的性质 | 实验三: 探究金属的活动性强弱 | 实验四:实验室制取二氧化碳 |
|
|
|
|
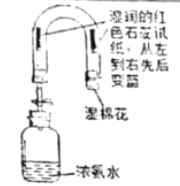
①实验一:说明分子具有的性质是_____________。
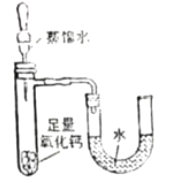
②实验二:观察到的现象是___________, 反应的化学方程式为_________。
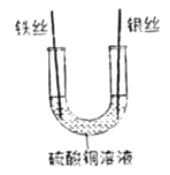
③实验三:能证明金属活动性Fe>Cu>Ag的现象是__________,反应一会儿后取出两种金属,溶液中溶质的存在情况是_________________。
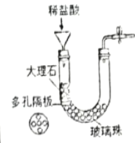
④实验四:为了达到“随开随用,随关随停”的要求,装置的改进措施是___________________。