��Ŀ����
����Ŀ��ij��ѧ����Χ�ơ�����кͷ�Ӧ������ѧ���ֳ�����С�飬����ʦ�����¿�չ̽����������ǽ�ѧƬ�Σ��������ѧϰ��������д�ո������пո�
����ʾʵ�顿��һ������ϡH2SO4���뵽ʢ��NaOH��Һ���ձ��С�
��ѧ�����ݡ��÷�Ӧ�Ļ�ѧ����ʽ ��
����̽��
��������⡿ʵ����δ�۲쵽����������ͬѧ���������ʣ���Ӧ����Һ��������ʲô�أ�
���� �롿������ʴ�ҷ�������롣����ͬѧ�IJ������£�
����һ��ֻ��Na2SO4 ���������Na2SO4��H2SO4
����������Na2SO4��NaOH �����ģ���Na2SO4��H2SO4��NaOH
����ͬѧ�����ϲ���������ɣ���Ϊ��һ�ֲ����Dz������ġ�����Ϊ�������IJ�������һ�ֲ�˵������ ��
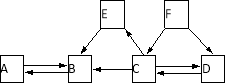
������ʵ�顿��1������ͬѧȡ�ձ��е�������Һ���Թ��У��μӼ���CuSO4��Һ�������Ա仯����Һ��һ��û�� ��
��2��Ϊ����֤������룬����ͬѧȡ�ձ��е���Һ����ѡ����ʦ�ṩ��pH��ֽ��ͭƬ��BaC12��Һ��Na2CO3��Һ���ֱ������������̽��ʵ�顣
ʵ�鷽�� | ����ҺpH | �μ�Na2CO3��Һ | �μ�BaCl2��Һ |
ʵ����� |
|
|
|
ʵ������ | ��ֽ��ɫ�����ձ�ɫ����pH��7 | ������ɫ���� | |
ʵ����� | ��Һ����H2SO4 | ��Һ����H2SO4 | ��Һ����H2SO4 |
���ó����ۡ�ͨ��̽����ȫ��ͬѧһ��ȷ�����������ȷ�ġ�
�����۷�˼����ʦ��ͬѧ�����ö��ַ�������̽�������ҵó���ȷ���۸���϶���ͬʱָ����������ʵ��̽���д����������Դ������ҷ�˼��ͬѧ�Ǿ�����˼����������������
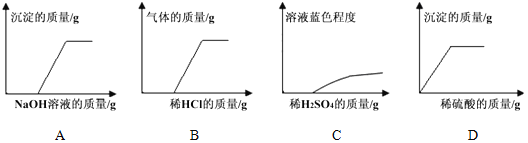
��1��ʵ����������Ե�һ�������� ��
��2��ʵ�鷽��̽����Ҳ��һ���Dz������ģ���������ԭ���� ��
II������̽��
ȡ��������ʾʵ�顿��Ӧ���ձ�������Һ100 g���������ʵ�飺
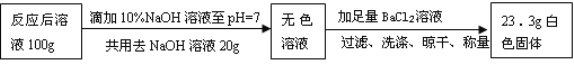
���㷴Ӧ����Һ��Na2SO4�����������Ƕ��٣������г�������̣�
��������ѧ�����ݡ�H2SO4+2NaOH = Na2SO4+ H2O�������롿������ ���ܹ��� ��������ʵ�顿��1��NaOH��2�������ݲ��� �����۷�˼����1��pH��ֽ����ֱ���������Һ������������������2��������Ҳ�ܺ��Ȼ�����Ӧ��������������֤�����������II��10.65%
��������
�����������һ������ϡH2SO4���뵽ʢ��NaOH��Һ���ձ��С���Ӧ�Ļ�ѧ����ʽH2SO4+2NaOH = Na2SO4+ H2O�������ϲ���������ɣ���Ϊ��һ�ֲ����Dz������ġ��������IJ����������ģ��������ܹ��� ������ͬѧȡ�ձ��е�������Һ���Թ��У��μӼ���CuSO4��Һ�������Ա仯����Һ��һ��û��NaOH������ᷴӦ�õ�����ɫ�ij������μ�Na2CO3��Һ�����ִ���������˵����Һ����H2SO4��ʵ����������Ե�һ��������pH��ֽ����ֱ���������Һ����ʵ�鷽��̽����Ҳ��һ���Dz������ģ���������ԭ����������Ҳ�ܺ��Ȼ�����Ӧ��������������֤��������ڣ�����Ӧ����Һ��Na2SO4������ΪX��
Na2SO4 + BaCl2 = 2NaCl + BaSO4��
142 233
X 23.3��
�б���ʽ����142��X=233:23.3�� ���X=14.2��
���������Ʒ�Ӧ��õ��������Ƶ�����ΪY��
2NaOH+ H2SO4= Na2SO4 + 2H2O
80 142
20����10% Y
�б���ʽ����80����20����10%��=142��Y ���Y=3.55��
��Ӧ����Һ��Na2SO4������������=��14.2��-3.55�ˣ���100����100%=10.65%��

 ������ϵ�д�
������ϵ�д� �żӾ���ϵ�д�
�żӾ���ϵ�д�