题目内容
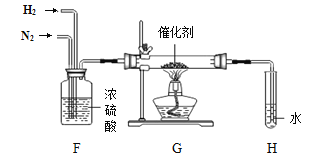
【题目】如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )

A. t1℃时将15g的乙物质加到50g水中充分溶解可得到65g的饱和溶液
B. t1℃时,甲.丙两种物质的溶液中溶质的质量分数一定相等
C. 将P点甲物质的溶液变为饱和溶液只能通过向溶液中增加甲物质的方法来实现
D. 将t1℃时三种物质的饱和溶液温度升高到t2℃,所得溶液溶质质量分数由大到小的顺序为:乙>甲>丙
【答案】D
【解析】
A. t1℃时,乙的溶解度小于30g;
B. t1℃时,甲、丙溶解度相同,但需要确定是饱和溶液才能确定质量分数相等;
C.不饱和到饱和途径:(1)增加溶质(2)蒸发溶剂(3)降温(大多数物质);
D.由 t1℃升高到t2℃,溶解度变大的,溶质质量分数保持不变。溶解度变小的,溶质质量分数减小至与t2℃饱和溶液溶质质量分数相等。
A. t1℃时,乙的溶解度小于30g,故将15g的乙物质加到50g水中充分溶解,形成的是饱和溶液,不可得到65g的饱和溶液,故A错误;
B. t1℃时,甲、丙两种物质的饱和溶液中溶质的质量分数一定相等,故B错误;
C.将P点甲物质的溶液变为饱和溶液,可以通过向溶液中增加甲物质的方法或是蒸发水分的方法来实现,故C错误;
D.将t1℃时三种物质的饱和溶液温度升高到t2℃,甲和乙的溶解度随温度的升高而增大,溶液组成不变,乙的溶质质量分数大于甲,而丙的溶解度随温度的升高而减小,溶质质量分数最小,故所得溶液溶质质量分数由大到小的顺序为:乙>甲>丙,故D正确;
答案选D。

 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
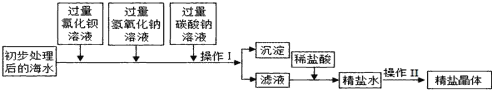
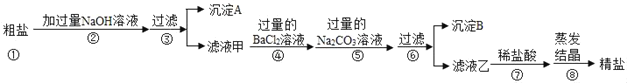
Happy holiday欢乐假期暑假作业广东人民出版社系列答案【题目】(7分)以电解食盐水为基础制取氯气、氢氧化钠等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不符合电解要求,因此必须经过精制。以粗盐为原料的“氯碱工业”流程如下:
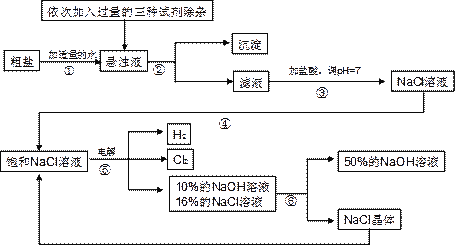
回答下列问题:
(1)氯气、氢氧化钠在工业上有广泛的用途。下列关于氢氧化钠的描述中,错误的是 。
A.能去除油污,可做厨房清洁剂 | B.易溶于水,溶解时放出大量的热 |
C.水溶液能使石蕊溶液变红 | D.可用作某些气体的干燥剂 |
(2)操作②的名称是 ,操作④的名称是 。
(3)操作①②间除杂质时所加的三种试剂是NaOH溶液、Na2CO3溶液、BaCl2溶液(均过量),其顺序要求是:Na2CO3溶液必须在BaCl2溶液之 (填“前”或“后”)加入。有同学提出用 溶液代替BaCl2溶液可达到同样的目的。
(4)电解饱和NaCl溶液的化学方程式是 。
(5)该流程中可以循环利用的物质是 。