题目内容
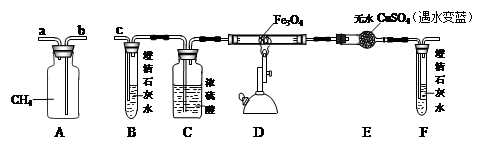
在小组活动中,王老师演示了一个实验:将烘干的碳酸镁与锌粉按照一定比例研细混匀,按照图1进行实验。然后指导同学们对碳酸镁与锌粉发生的反应进行了实验探究。
【查阅资料】部分含有镁、锌元素物质的相关性质。
①氧化镁、氧化锌:均为白色固体,均与盐酸反应,生成无色盐溶液。
②碳酸镁、碳酸锌:均为白色固体,均与盐酸反应,生成无色盐溶液和二氧化碳气体。
【实验探究】
(1)实验一:碳酸镁与锌粉反应的气体产物是什么?
结论:碳酸镁与锌粉反应的气体产物是 。②中气体燃烧的化学方程式为 。


图1 图2
(2)实验二:碳酸镁与锌粉反应的固体产物是什么?
王老师将剩余固体分成2份,由甲、乙两组同学进行探究。
甲组同学将剩余固体直接按照图2进行实验,观察到A中有大量气泡生成,B中的澄清石灰水变浑浊,将产生的气体在C处验纯后点燃,观察到淡蓝色火焰。C处点燃的气体是 (填化学式)。甲组同学获得结论:该反应的固体产物是碳酸锌和镁。
乙组同学将剩余固体先进行了处理,然后也按照图2进行了实验,观察到A中固体溶解,生成无色溶液,B中没有明显变化。他们对剩余固体的处理操作是 。乙组同学利用质量守恒定律和实验现象,分析碳酸镁与锌粉发生反应后的固体产物是氧化锌和氧化镁,其理由是 。
(3)实验反思:老师看到两组同学的实验报告后,确定乙组的结论是正确的,碳酸镁与锌粉反应的化学方程式为 。同学们对甲组的实验过程再次进行了分析,由B、C处产生的现象,可以说明甲组放入试管A中的固体成分含有 。
【查阅资料】部分含有镁、锌元素物质的相关性质。
①氧化镁、氧化锌:均为白色固体,均与盐酸反应,生成无色盐溶液。
②碳酸镁、碳酸锌:均为白色固体,均与盐酸反应,生成无色盐溶液和二氧化碳气体。
【实验探究】
(1)实验一:碳酸镁与锌粉反应的气体产物是什么?
| 序号 | 实验操作 | 实验现象 |
| ① | 收集两瓶气体,盖好玻璃片。向其中一瓶迅速倒入少量澄清石灰水,盖好振荡。 | 无明显现象。 |
| ② | 将另一瓶气体点燃,待火焰熄灭后,迅速倒入少量澄清石灰水,盖好振荡。 | 气体安静燃烧,火焰呈蓝色,澄清石灰水变浑浊。 |


图1 图2
(2)实验二:碳酸镁与锌粉反应的固体产物是什么?
王老师将剩余固体分成2份,由甲、乙两组同学进行探究。
甲组同学将剩余固体直接按照图2进行实验,观察到A中有大量气泡生成,B中的澄清石灰水变浑浊,将产生的气体在C处验纯后点燃,观察到淡蓝色火焰。C处点燃的气体是 (填化学式)。甲组同学获得结论:该反应的固体产物是碳酸锌和镁。
乙组同学将剩余固体先进行了处理,然后也按照图2进行了实验,观察到A中固体溶解,生成无色溶液,B中没有明显变化。他们对剩余固体的处理操作是 。乙组同学利用质量守恒定律和实验现象,分析碳酸镁与锌粉发生反应后的固体产物是氧化锌和氧化镁,其理由是 。
(3)实验反思:老师看到两组同学的实验报告后,确定乙组的结论是正确的,碳酸镁与锌粉反应的化学方程式为 。同学们对甲组的实验过程再次进行了分析,由B、C处产生的现象,可以说明甲组放入试管A中的固体成分含有 。
(1)CO 2CO+O2 ===2CO2
(2)H2 继续按图1方式加热,直至不再产生气体
依据质量守恒定律,反应物和生成物中的元素有C、Mg、Zn和O元素,依据实验现象C元素的产物为CO,Mg、Zn元素对应的固体产物中没有碳酸镁、碳酸锌、镁粉、锌粉存在,所以Mg、Zn元素对应固体产物只能是氧化锌和氧化镁。 (2分)
(3)MgCO3 + Zn ="===" MgO + ZnO + CO↑
MgCO3、Zn、MgO、ZnO(MgCO3、Zn为给分点)
(2)H2 继续按图1方式加热,直至不再产生气体
依据质量守恒定律,反应物和生成物中的元素有C、Mg、Zn和O元素,依据实验现象C元素的产物为CO,Mg、Zn元素对应的固体产物中没有碳酸镁、碳酸锌、镁粉、锌粉存在,所以Mg、Zn元素对应固体产物只能是氧化锌和氧化镁。 (2分)
(3)MgCO3 + Zn ="===" MgO + ZnO + CO↑
MgCO3、Zn、MgO、ZnO(MgCO3、Zn为给分点)
(1)由于该气体燃烧后能生成使澄清石灰水变浑浊的气体可知该气体是一氧化碳,
(2)碳酸锌和盐酸反应能生成二氧化碳,镁与盐酸反应可以生成氢气,所以加入盐酸能生成可燃气体是氢气,使澄清石灰水变浑浊的气体是二氧化碳
由于乙组同学的实验现象是A中固体溶解,生成无色溶液,B中没有明显变化,所以可判断乙组对剩余固体的处理是继续加热至不在生成气体为止,此时固体中无碳酸锌和镁,依据质量守恒定律,反应物和生成物中的元素有C、Mg、Zn和O元素,依据实验现象C元素的产物为CO,Mg、Zn元素对应的固体产物中没有碳酸镁、碳酸锌、镁粉、锌粉存在,所以Mg、Zn元素对应固体产物只能是氧化锌和氧化镁
(3)结合以上结论可知碳酸镁与锌粉反应会生成一氧化碳、氧化镁和氧化锌,因此可判定甲组放入试管A中的固体成分含有MgCO3、Zn、MgO、ZnO的混合物
(2)碳酸锌和盐酸反应能生成二氧化碳,镁与盐酸反应可以生成氢气,所以加入盐酸能生成可燃气体是氢气,使澄清石灰水变浑浊的气体是二氧化碳
由于乙组同学的实验现象是A中固体溶解,生成无色溶液,B中没有明显变化,所以可判断乙组对剩余固体的处理是继续加热至不在生成气体为止,此时固体中无碳酸锌和镁,依据质量守恒定律,反应物和生成物中的元素有C、Mg、Zn和O元素,依据实验现象C元素的产物为CO,Mg、Zn元素对应的固体产物中没有碳酸镁、碳酸锌、镁粉、锌粉存在,所以Mg、Zn元素对应固体产物只能是氧化锌和氧化镁
(3)结合以上结论可知碳酸镁与锌粉反应会生成一氧化碳、氧化镁和氧化锌,因此可判定甲组放入试管A中的固体成分含有MgCO3、Zn、MgO、ZnO的混合物

练习册系列答案
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目