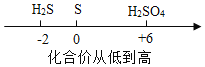
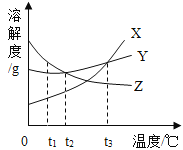
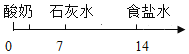��Ŀ����
����Ŀ�������(C4H9Li)���ϳɹ�ҵ��һ�ֳ��õİ�ɫ��ĩ�Լ����۵㩁95�棬�е�80�棬��ˮ������������ȼ����Է�֮������64�����й��ڶ���﮵�˵����ȷ����( )
A. ���������4��̼ԭ�ӡ�9����ԭ�ӡ�1���ԭ�ӹ��ɵ�
B. �������̼Ԫ����������Ϊ75%
C. ����������ʹ�ù������������ȼ�գ�������ˮ����
D. ��������л��߷��Ӳ���
���𰸡�B
��������
A����������ɷ��ӹ��ɵģ���������ԭ��ֱ�ӹ��ɵģ��ʴ���
B���������̼Ԫ����������Ϊ![]() ��100%=75%������ȷ��
��100%=75%������ȷ��
C���������ˮ����ȼ�������������ʹ�ù������������ȼ�գ�������ˮ���𣬹ʴ���
D���л��߷��ӻ��������Է�����������������ʮ������﮵���Է�������Ϊ12��4+1��9+7=64�����Բ������л��߷��ӻ�����ʴ���
��ѡ��B��

����Ŀ���±�Ϊ�Ȼ��ơ�̼������ˮ�е��ܽ�ȡ��ҹ����������кܶ���ˮ�������������Dz��ľ��صIJ�����γء�ij�κ�������ũ��ͨ���������̼�.����ɹ�Ρ���ô������Ρ�����ġ��ָ����(��Ҫ�ɷ���̼����) ����ָ�Ȼ��ơ�
�¶�/�� | 0 | 10 | 20 | 30 | 40 | |
�ܽ�� | �Ȼ��� | 35.7 | 35.8 | 35.9 | 36.1 | 37.1 |
̼���� | 7.0 | 12.5 | 21.5 | 39.7 | 49.0 | |
(1)���ͼ����Ҫ�����������̼����ɹ�Ρ����еĵ���____��
(2)С��ͬѧȡ�ú�����Ʒ����̽����
��������⣩�ú�����Ʒ�ijɷ���ʲô?
����������裩����һ:ֻ��Na2CO3:�����:ֻ��NaCl��������:Na2CO3��NaCl��
��ʵ��̽����
ʵ����� | ʵ������ | ʵ����� |
ȡ������Ʒ���Թ��У������м���������____��Һ�����ˣ��ó�������Һ��������м�������ϡ���� | ������ɫ���� ���ְ�ɫ������ʧ | ���������� |
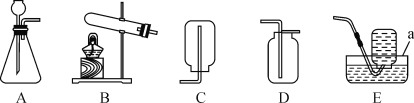
����չ���죩Ϊ��һ��ȷ���ú�����Ʒ��Na2CO3������������С��ͬѧ��ȡ�ú�����Ʒ10.00g������ͼ��ʾ�IJ���ʵ��(�ٶ�ÿ������ȫ��Ӧ������)��

�ٷ�Ӧ����֮��ͨ������������Ŀ����_____��
��װ��A������������Һ��������_____(�û�ѧ����ʽ��ʾ)��
��ʵ���������װ��E����0.44g���������ͼ��ʾ��ʵ����̺��ṩ�����ݼ���ú�����Ʒ��̼���Ƶ����������Ƕ���_____?(д�����㲽�裬��������ȷ��0.1%)
����Ŀ����һ�������Ҵ���C2H6O������������һ����յ���������ȼ����÷�Ӧǰ������ʵ��������±���
���� | �Ҵ� | ���� | ˮ | ������̼ | X |
��Ӧǰ����/g | 4.6 | 8.0 | 0 | 0 | 0 |
��Ӧ������/g | 0 | 0 | 5.4 | 4.4 | a |
�����ж���ȷ���ǣ� ��
A. ����a��ֵΪ2.6
B. Xһ���Ǹ÷�Ӧ�Ĵ���
C. X���ܺ�����Ԫ��
D. ����ʼʱ������������9.6g������X����
����Ŀ��Ϊ�Ƚ�4�ֽ���X��Y��Z��W�Ļ�ԣ�С�ս�����һϵ��ʵ�飬��������ʾ![]() �����ܷ�Ӧ�ļ�Ϊ��
�����ܷ�Ӧ�ļ�Ϊ��![]() �������ܷ�Ӧ�ļ�Ϊ��
�������ܷ�Ӧ�ļ�Ϊ��![]() �����ޱ�ǵı�ʾδ����ʵ�飮�����ǵĽ������˳��Ϊ
�����ޱ�ǵı�ʾδ����ʵ�飮�����ǵĽ������˳��Ϊ![]()
�μӷ�Ӧ������ | X | Y | Z | W |
|
|
|
| |
|
|
| ||
ϡ���� |
|
|
|
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()