��Ŀ����
����Ŀ����ʽ̼��þ[Mg2(OH)2CO3]������þ(MgO2)������Ҫ����ԭ�ϡ�
�� ��Mg2(OH)2CO3Ϊԭ�ϣ��Ʊ���ƷMgO2�IJ������£�
��1������ ����Mg2(OH)2CO3�õ��������������һ�ֳ����������壬����ʹ����ʯ��ˮ����ǡ�����ʱ��Ӧ�Ļ�ѧ����ʽΪ ��
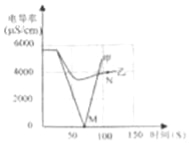
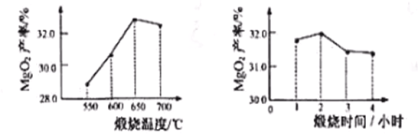
��2��ת�� �����ù����м�˫��ˮ��ֽ��裬������ӦMgO+H2O2=MgO2+H2O���¶����ߣ�˵���÷�Ӧ ����(��ų��������ա�)������������ͬ�������¶ȡ�����ʱ�䲻ͬ������MgO��MgO2����(����=![]() ��100%)��Ӱ��ֱ���ͼ��ʾ������ѵ������¶�Ϊ ��������ʱ��Ϊ Сʱ��
��100%)��Ӱ��ֱ���ͼ��ʾ������ѵ������¶�Ϊ ��������ʱ��Ϊ Сʱ��
��3������ �õ���Ʒ
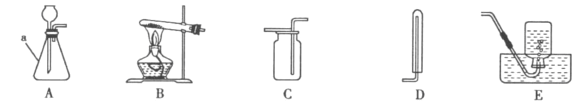
��4���ⶨ �����Ʒ�н���������MnO��ijС���������װ�ã�ͨ���ⶨ����O2�����������MgO2������������
��֪��A��MnO2��ϡ�����Ӧ B��MgO2+2HCl=MgCl2+H2O2
C��2MgO2![]() 2MnO+O2�� D��MgO+C
2MnO+O2�� D��MgO+C![]() Mg+CO��
Mg+CO��
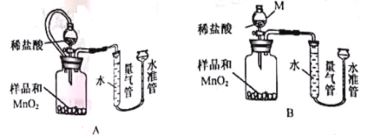
������M�������� ��MnO2�������� ��
����ͬ�����£� ��ʹ�ⶨ�����ȷ��(�װ��A����װ��B��)
��ʵ������������������Ϊ37%���ܶ���1.18g��mL-1��Ũ��������10%��ϡ����110g����Ҫˮ mL��(ˮ���ܶ���1g��mL-1������������һλС��)
�������ۣ���С�������������3�ַ������ֱ�ȡ5.0g��Ʒ����ʵ�飬��ȷ��MgO2������������ ��(�����)
A�����ȣ�ʹMgO2��ȫ�ֽ⣬���ʣ����������
B��������̿���ڸ����³�ַ�Ӧ���������Mg������
C���ȼ�����ϡ���ᣬ�ټ�����NaOH��Һ����ַ�Ӧ�����Mg(OH)2����
�� MgCl2���Ʊ�Mg2(OH)2CO3��ԭ�ϡ����ú�̼��þ84%����þ���Ʊ�MgCl2����Ӧ���£�
MgCO3+Cl2+CO![]() MgCl2+2CO2(�����ʲ��μӷ�Ӧ)������19��MgCl2��Ҫ��������þ����ٶ֣�(д���������)
MgCl2+2CO2(�����ʲ��μӷ�Ӧ)������19��MgCl2��Ҫ��������þ����ٶ֣�(д���������)
���𰸡���1�� Mg2(OH)2CO3![]() 2MgO+CO2��+H2O�� ��2���ų� 650 2 ��4������Һ©�� �� ��A ��80.3 ��a �� 16.8t
2MgO+CO2��+H2O�� ��2���ų� 650 2 ��4������Һ©�� �� ��A ��80.3 ��a �� 16.8t
����������1�� ����Mg2(OH)2CO3�õ��������������һ�ֳ����������壬����ʹ����ʯ��ˮ����ǡ�����ʱ��Ӧ�Ļ�ѧ����ʽΪMg2(OH)2CO3![]() 2MgO+CO2��+H2O����2�� �����ù����м�˫��ˮ��ֽ��裬������ӦMgO+H2O2=MgO2+H2O���¶����ߣ�˵���÷�Ӧ�ų���������������ͼ��֪��ѵ������¶�Ϊ650��������ʱ��Ϊ2Сʱ����4���ⶨ������M�������Ƿ�Һ©����MnO2�������Ǵ����ã�����ͬ�����£�Aװ����ʹ�ⶨ�����ȷ����ΪAװ������ƽ����ѹ��װ�ã���ʵ������������������Ϊ37%���ܶ���1.18g��mL-1��Ũ��������10%��ϡ����110g����Ҫˮ������ Ϊ;110g-(10%��110g)/37%=80.3g;���ֱ�ȡ5.0g��Ʒ����ʵ�飬��ȷ��MgO2������������A�����ȣ�ʹMgO2��ȫ�ֽ⣬���ʣ����������;������19��MgCl2��Ҫ��������þ��Ϊx
2MgO+CO2��+H2O����2�� �����ù����м�˫��ˮ��ֽ��裬������ӦMgO+H2O2=MgO2+H2O���¶����ߣ�˵���÷�Ӧ�ų���������������ͼ��֪��ѵ������¶�Ϊ650��������ʱ��Ϊ2Сʱ����4���ⶨ������M�������Ƿ�Һ©����MnO2�������Ǵ����ã�����ͬ�����£�Aװ����ʹ�ⶨ�����ȷ����ΪAװ������ƽ����ѹ��װ�ã���ʵ������������������Ϊ37%���ܶ���1.18g��mL-1��Ũ��������10%��ϡ����110g����Ҫˮ������ Ϊ;110g-(10%��110g)/37%=80.3g;���ֱ�ȡ5.0g��Ʒ����ʵ�飬��ȷ��MgO2������������A�����ȣ�ʹMgO2��ȫ�ֽ⣬���ʣ����������;������19��MgCl2��Ҫ��������þ��Ϊx
MgCO3+Cl2+CO![]() MgCl2+2CO2
MgCl2+2CO2
84 95
X 19t
84/x=95/19t
t=16.8t
������19��MgCl2��Ҫ��������þ��16.8t

 �����Ƹ���ʦ����ϵ�д�
�����Ƹ���ʦ����ϵ�д� ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д� ����С����ͬ������ϵ�д�
����С����ͬ������ϵ�д�