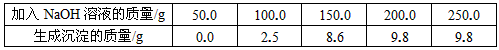
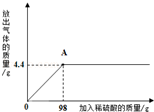
题目内容
若要生产含杂质4%的生铁100 t,需要含氧化铁60%的赤铁矿石的质量是多少?(要求:写出计算过程,计算结果保留小数点后1位)
228.6t
解析试题分析:含杂质物质的计算要把混合物的质量转化为纯物质的质量,即纯物质质量=含杂质物质质量×纯度,再把纯物质的质量带入化学方程式计算。最后再把计算出的纯物质质量转换为含杂质物质的质量。
[解]设:需要向炼铁高炉中投入这种铁矿石的质量为x
Fe2O3 + 3CO  2Fe + 3CO2
2Fe + 3CO2
160 112
60%x (1-4%)×100 t =
= 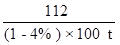
x=" 228.6" t
答:需要向炼铁高炉中投入这种铁矿石的质量为228.6t。
考点:含杂质的物质利用化学方程式的计算

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目