题目内容
【题目】下列有关质量守恒定律的理解中,正确的是 ( )
A.5g盐溶解在100g水中形成105g溶液遵循质量守恒定律
B.化学反应前后分子的总数一定不会发生变化
C.镁条燃烧后质量增加,不遵循质量守恒定律
D.制硅流程中一个化学反应方程式为2H2+SiCl4![]() Si+4X是,则X的化学式为HCl
Si+4X是,则X的化学式为HCl
【答案】D
【解析】
在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.所以质量守恒定律只能用来解释化学反应,可以据此解答。
A、盐溶解在水中属于物理变化,所以虽然混合后质量不变,但是不能用质量守恒定律来解释,故错误;
B、根据化学变化的实质可以知道,在化学变化中是分子破裂成原子,原子重新组合成新的分子,在原子重新组合的过程中,分子的总数可能发生改变,故错误;
C、镁条燃烧是和空气中的氧气发生了反应,所以反应后生成物的质量应该等于参加反应的镁和氧气的质量之和,所以遵守质量守恒定律,故错误;
D、根据质量守恒定律的元素守恒、原子种类和个数不变,结合反应的化学方程式为:2H2+SiCl4![]() Si+4X,反应前H原子个数为4个,Si原子个数为1个,Cl原子个数为4个;反应后Si原子个数为1个,故推测X中有1个H原子和1个Cl原子,为HCl.故正确;
Si+4X,反应前H原子个数为4个,Si原子个数为1个,Cl原子个数为4个;反应后Si原子个数为1个,故推测X中有1个H原子和1个Cl原子,为HCl.故正确;
故选:D。

 字词句段篇系列答案
字词句段篇系列答案【题目】分类、类比、推理都是学习化学常用的方法。
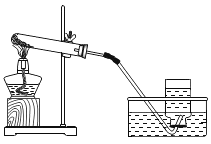
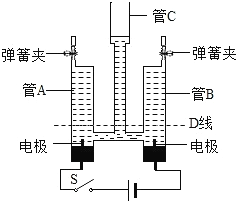
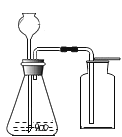
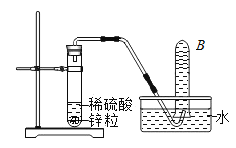
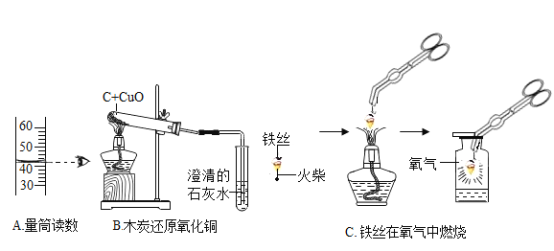
(1)实验室制备某些气体的实验中,都能达到实验目的,但是其方案都有所不同,请从实验是否安全,操作是否简便,是否节约能源,是否环保等方面考虑,据此应将下列实验中的D与_____(填“A”或“B”或“C”)归为一类,依据是_____。
加热高锰酸钾制氧气 | 电解水制氢气 | 大理石和稀盐酸制二氧化碳 | 锌和硫酸制氢气 |
|
|
|
|
A | B | C | D |
(2)今年春节期间,新冠肺炎席卷全国,为了防止疫情护散,人们使用了“84”高效消毒液,其主要成分为次氯酸钠(NaCIO),广泛用于机场、车站、宾馆,医院等公共场所的卫生消毒,制取次氯酸钠发生反应的化学方程式为![]() ,其中_____元素的化合价在化学反应前后既有升高义有降低。请你再写出一个符合在同一种物质中有一种元素的化合价在化学反应前后既有升高又有降低的反应的化学方程式_____(初中学过的)。
,其中_____元素的化合价在化学反应前后既有升高义有降低。请你再写出一个符合在同一种物质中有一种元素的化合价在化学反应前后既有升高又有降低的反应的化学方程式_____(初中学过的)。