题目内容
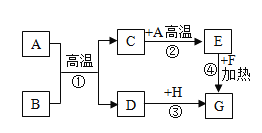
【题目】某化合物的浓溶液有强烈的腐蚀性,实验室中常用作气体的干燥剂,其稀溶液X具有如下转化关系。A、B、C、D、E、F、G、M、N都是初中常见的化学物质。已知:B、C、F都是氧化物,通常状况下它们分别是无色无味液体、无色无味气体和黑色粉末状固体;G是通常状况下密度最小的气体。(图中部分反应物、生成物已略去)。请回答下列问题:
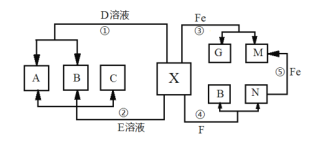
(1)写出化学式:G____________,X______________;
(2)写出化学反应的类型:反应⑤_________________;
(3)写出符合题意的化学方程式:
反应②________________________________________________;
反应③_________________________________________________;
反应④_________________________________________________。
【答案】H2 H2SO4 置换反应 H2SO4+Na2CO3=Na2SO4+CO2↑+H2O H2SO4+Fe=FeSO4+H2↑ H2SO4+CuO=CuSO4+H2O
【解析】
某化合物的浓溶液有强烈的腐蚀性,实验室中常用作气体的干燥剂,因此是浓硫酸,X是稀硫酸;G是通常状况下密度最小的气体,因此G是氢气;稀硫酸有五种化学性质,即硫酸与指示剂反应,硫酸与金属反应,硫酸与金属氧化物反应,硫酸与碱反应,硫酸与盐反应;③是铁与硫酸反应生成硫酸亚铁和氢气;因为F是黑色粉末状固体,属于氧化物,因此F是氧化铜;氧化铜和硫酸反应生成硫酸铜和水,B、C、F都是氧化物,因此B是水,N是硫酸铜,⑤铁和硫酸铜反应生成硫酸亚铁和铜,因此属于置换反应;由流程图和硫酸的性质可知,D是碱,E是碳酸盐,因此②可以是:碳酸钠和硫酸反应生成硫酸钠和水和二氧化碳。
(1)某化合物的浓溶液有强烈的腐蚀性,实验室中常用作气体的干燥剂,因此是浓硫酸,X是稀硫酸;G是通常状况下密度最小的气体,因此G是氢气;故答案为:H2;H2SO4
(2)反应⑤是铁和硫酸铜反应生成硫酸亚铁和铜,是由一种单质和一种化合物生成另一种单质和另一种化合物,因此属于置换反应;
(3)由流程图和硫酸的性质可知,D是碱,E是碳酸盐,因此②可以是:碳酸钠和硫酸反应生成硫酸钠和水和二氧化碳;③是铁与硫酸反应生成硫酸亚铁和氢气;因为F是黑色粉末状固体,属于氧化物,因此F是氧化铜;反应④是氧化铜和硫酸反应生成硫酸铜和水;故答案为:H2SO4+Na2CO3═Na2SO4+CO2↑+H2O(其他合理答案也可);H2SO4+Fe═FeSO4+H2↑;H2SO4+CuO═CuSO4+H2O。

 阅读快车系列答案
阅读快车系列答案【题目】某实验小组的同学为了测定CaCl2和NaCl的混合物中CaCl2的含量,他们取样品25.8g于烧杯中,加入134.2g水全部溶解,再多次加入某Na2CO3溶液充分反应。加入Na2CO3溶液 与产生沉淀的质量如下表所示:
Na2CO3溶液/g | 10 | 10 | 10 | 10 | 10 | 10 |
沉淀质量/g | 5 | 10 | 15 | 20 | 20 | m |
(1)Na2CO3中钠、碳、氧三种元素的质量比为_____,表中m=_____。
(2)样品中CaCl2的质量是____;恰好完全反应时,所得溶液中溶质的质量分数是____。