题目内容
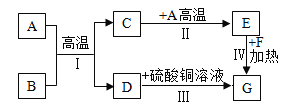
【题目】A~H 是初中化学常见的物质。已知 A 为黑色固体单质,G 为红色固体单质,B 为红棕色粉末,F 为黑色粉末,它们的转化关系如下图所示。请回答:
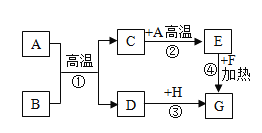
(1)B 的化学式为_______。
(2)反应①的化学方程式为_____________;写一个能实现反应③的化学方程式____________。
(3)反应涉及的化学反应基本类型是_______________。
【答案】![]()
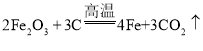
![]() 化合反应
化合反应
【解析】
根据常见的红色固体有铜、氧化铁等,根据题干提供的信息,本题的解题突破口是G为红色固体单质,则G是铜,A为黑色固体单质,B为红棕色粉末,A和B高温能反应生成C和D,则A是碳,B是氧化铁,生成的D能与H反应铜,则D是铁,H可能是硫酸铜,C是二氧化碳,C能与A反应生成E,则E是一氧化碳,一氧化碳与F反应生成铜,则F是氧化铜,据此解答。
(1)根据上述分析可知,B是![]() 。
。
(2)反应①为C与![]() 反应生成铁与二氧化碳,反应的化学方程式为
反应生成铁与二氧化碳,反应的化学方程式为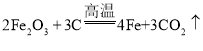 ;反应③为铁和硫酸铜转化成铜和硫酸亚铁,能实现反应③的化学方程式为
;反应③为铁和硫酸铜转化成铜和硫酸亚铁,能实现反应③的化学方程式为![]() 。
。
(3)反应②为C与CO2在高温条件下反应生成CO,涉及的化学反应基本类型是化合反应。

【题目】实验室有一瓶没有密封好的氢氧化钠固体,为了验证其是否变质,同学们对这瓶固体成分进行了下列实验探究。
(查阅资料)Na2CO3溶液呈碱性,CaCl2溶液呈中性
(提出猜想)
猜想Ⅰ:固体全部是NaOH;
猜想Ⅱ:固体全部是______________;
猜想Ⅲ:固体是NaOH和Na2CO3的混合物。
(进行实验):
实验操作步骤 | 实验现象 | 结论及化学方程式 |
步骤1:取少量固体于试管中,加水溶解,滴入足量稀盐酸 | ______________ | 猜想Ⅰ不成立。 |
步骤2:另取少量固体于试管中,加水充分溶解,再滴加过量氯化钙溶液 | ______________ | 猜想Ⅱ或Ⅲ成立。 反应的化学方程式为: _______________________________ |
步骤3:取步骤2反应后的上层清液于试管中,滴入无色酚酞试液 | 若酚酞不变红色 | 猜想________成立 |
若酚酞变红色 | 猜想________成立 |
(问题讨论)步骤2中滴加氯化钙溶液必须“过量”的原因是________________。
(反思与交流)久置的固体氢氧化钠变质的原因是(用化学方程式表示)______________。