题目内容
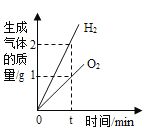
【题目】向某盐酸和氯化镁的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液质量的关系如图所示。下列说法正确的是
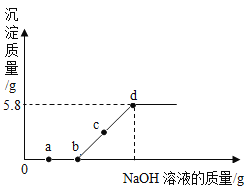
A.a点时,溶液pH>7
B.c点时,溶液中含有两种溶质
C.b点时,溶液质量比原混合溶液质量小
D.d点时,整个反应过程消耗的氢氧化钠溶液质量为8g
【答案】B
【解析】
A. 向某盐酸和氯化镁的混合溶液中加入某浓度的氢氧化钠溶液,先后发生的反应分别是:NaOH+HCl=NaCl+H2O,MgCl2+2NaOH=Mg(OH)2↓+2NaCl,a点时,盐酸没有完全反应,溶液显酸性,pH<7,故A错误;
B. c点时,是氢氧化钠和氯化镁反应,溶液中含有氯化镁和生成的氯化钠两种溶质,故B正确;
C. b点时,氢氧化钠与盐酸恰好反应,因为反应中无气体、沉淀生成,所以溶液质量大于原混合溶液质量,故C错误;
D. d点时,生成了8g氢氧化镁沉淀,设与氯化镁反应的氢氧化钠的质量为x。
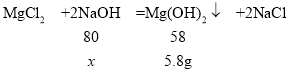
![]() ,解得x=8g
,解得x=8g
整个反应过程消耗的氢氧化钠溶液质量包括与盐酸反应的氢氧化钠溶液质量与氯化镁反应的氢氧化钠溶液质量,所以整个反应过程消耗的氢氧化钠溶液质量>8g,故D错误。
故选B。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案【题目】下表是几种物质在20℃的溶解度和相对分子质量。回答下列问题:
物质 | NaCl | NaHCO3 | NH4Cl | NH4HCO3 |
溶解度/g | 36.0 | 9.6 | 37.2 | 21.0 |
相对分子质量 | 58.5 | 84 | 53.5 | 79 |
(1)20℃时,用50g蒸馏水配制饱和NaHCO3溶液。
①计算需称量NaHCO3的质量是_____g。
②将称量的NaHCO3固体倒入盛有50g蒸馏水的烧杯中,然后用_____(填仪器名称)不断搅拌,直至_____。
③用配制所得的溶液可处理溶质的质量分数为1%的稀H2SO4_____g。
(2)相同温度下,不同溶质同时溶解在同一溶剂中,溶解度不变。在20℃时,将11.7gNaCl固体和15.8gNH4HCO3固体同时放入盛有100g水的烧杯中,充分搅拌,静置,观察到烧杯底部有晶体出现,该过程只发生复分解反应。杯底的晶体是_____,杯底晶体的质量是_____g。
【题目】下表是硝酸钾和氯化铵在不同温度时的溶解度。分析表中数据,回答问题。
温度/℃ | 0 | 20 | 40 | 60 | |
溶解度/g | 硝酸钾 | 13.3 | 31.6 | 63.9 | 110 |
氯化铵 | 29.4 | 37.2 | 45.8 | 55.2 | |
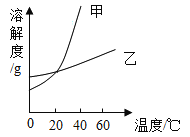
(1)上图中,甲可表示___(填化学式)的溶解度曲线。
(2)40℃时,两种物质的饱和溶液中,溶质质量分数较小的是__(填化学式)。
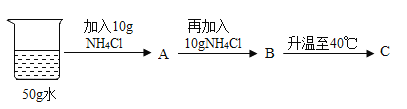
(3)20℃时,按下图所示操作,B中溶液的溶质与溶剂质量比为_____(填最简整数比);C中的溶液是__(填“饱和”或“不饱和”)溶液。
(4)60℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到60℃,剩余溶液的质量:硝酸钾溶液__(填“>”“<”或“=”)氯化铵溶液。
(5)室温下,将盛有硝酸钾的饱和溶液的试管放入盛有水的烧杯中,再向烧杯内的水中加入一定量的硝酸铵并搅拌,试管内可以观察到的现象是____。