题目内容
【题目】某氯化钠样品中含有少量的氯化钙,样品中钠元素和钙元素的质量比为23:20。取一定量的该样品,向其中加入适量的碳酸钠溶液(密度为1.1g/cm3)恰好完全反应,过滤,得到10g沉淀和112.8g滤液。请计算:
(1)原样品中氯化钙的质量
(2)所加入碳酸钠溶液的溶质质量分数。
(3)所加入碳酸钠溶液的体积。(计算结果精确到0.1)
【答案】(1)11.1g;(2)10.6%;(3)90.9ml
【解析】
(1)设样品中含有氯化钙的质量为x,所加碳酸钠溶液中的溶质质量为y
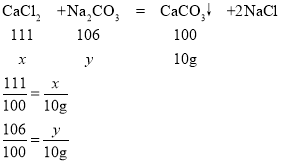
x=11.1g
y=10.6g
答:原样品中氯化钙的质量为11.1g。
(2)设11.1g氯化钙中含有的钙元素质量为m
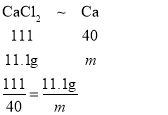
m=4g
样品中钠元素和钙元素的质量比为23:20,所以
样品中的钠元素为![]()
则样品中氯化钠的质量为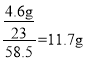
所以原样品的质量=![]() ,
,
则加入的碳酸钠溶液质量=![]()
所加碳酸钠溶液的溶质质量分数![]()
答:所加入碳酸钠溶液的溶质质量分数为10.6%。
(3)加入碳酸钠溶液的体积为![]()
答:所加入碳酸钠溶液的体积为90.9mL。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目