题目内容
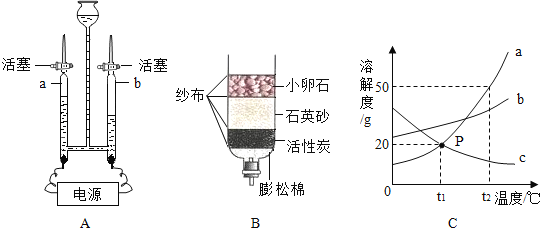
【题目】根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
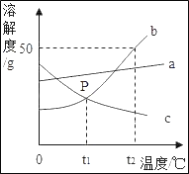
(1)P点表示在t1℃两物质的溶解度关系为b_____c(填“>”、“<”或“=”).
(2)t2℃,a、b、c三种物质的饱和溶液溶质质量分数的大小关系为_____.
(3)t2℃时,50g b物质加入到50g水中充分溶解后,所得溶液的质量为_____.
(4)b中含有少量的a,若要提纯b,可采用_____结晶的方法.把c物质的不饱和溶液变为饱和溶液,下列有关说法不正确的是_____ (填序号,下同)
A 溶剂的质量可能变小
B 溶质的质量一定不变
C 溶质的质量分数可能变大
D 溶液的质量可能变小
E 该饱和溶液还可以溶解其它物质
(5)把100g质量分数为98%的浓硫酸稀释成10%的稀硫酸,需要水的质量是_____g.
【答案】= b>a>c 75g 降温 B 880
【解析】
(1)溶解度曲线的交点表示该温度下两物质的溶解度相等;
(2)饱和溶液中溶质质量分数的计算式![]() ×100%,即溶解度大则溶质的质量分数大;
×100%,即溶解度大则溶质的质量分数大;
(3)据该温度下b的溶解度分析解答;
(4)据物质的溶解度随温度变化情况分析提纯物质的方法;c的溶解度随温度升高而减小,所以使其不饱和溶液变为饱和溶液,可采取加入溶质、蒸发溶剂、升温的方法,并结合饱和溶液概念及选项解答;
(5)稀释过程中溶质的质量不变.
(1)P点是t1℃两物质的溶解度曲线 的交点,表示二者的溶解度关系是:b=c;
(2)t2℃,a、b、c三种物质的溶解度大小关系是:b>a>c,饱和溶液中溶解度大则溶质的质量分数大,故饱和溶液溶质质量分数的大小关系为 b>a>c;
(3)t2℃时b的溶解度是50g,即100g水中最多溶解50g的b,所以50g b物质加入到50g水中充分溶解后,最多溶解25g,故所得溶液的质量为 75g;
(4)a的溶解度受温度影响不大,b的溶解度受温度影响较大,所以b中含有少量的a,若要提纯b,可采用 降温结晶的方法;
把c的溶解度随温度升高而减小,所以使其不饱和溶液变为饱和溶液,可采取加入溶质、蒸发溶剂、升温的方法;
A.若采取蒸发溶剂的方法,则溶剂的质量变小,正确;
B.若采取升温至恰好饱和的方法,则溶液中溶质的质量不变,故错误;
C.若采取蒸发溶剂的方法,则溶剂的质量变小,溶质的质量不变,溶质的质量分数变大,正确;
D.蒸发溶剂的方法,则溶剂的质量变小,溶液的质量变小,正确;
E.c的饱和溶液是该温度下再加入c不能溶解,但还可以溶解其它物质,是其他物质的不饱和溶液,正确;
(5)把100g质量分数为98%的浓硫酸稀释成10%的稀硫酸,设需要水的质量是x,则有100g×98%=(100g+x)×10%,解得x=880g;
故答案为:(1)=;(2)b>a>c;(3)75g;(4)降温;B;(5)880.

 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案【题目】某研究小组对自动充气气球(示意图如下)进行下列探究。
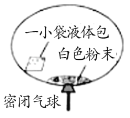
(查阅资料)该反应充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气。
(1)通常用澄清的石灰水来检验气体是二氧化碳,该反应的化学方程式 为_____。
(2)室温时,用pH试纸测得溶液的pH=3,该溶液呈_____性。
(3)探究白色粉末成分:
(猜想与假设)甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠。
(设计并进行实验)
实验一:完成下表:
操作步骤 | 现象 | 结论 |
_____ | _____ | 甲同学的猜想不正确 |
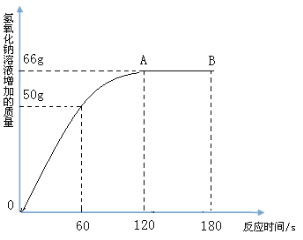
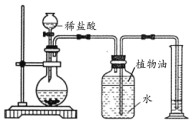
实验二:室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的稀盐酸,并测量生成二氧化碳的体积(装置如图),记录如下表:
实验编号 | 锥形瓶内物质 | 最终得到CO2体积/mL | |
名称 | 质量/g | ||
① | 碳酸氢钠 | 0.8 | V1 |
② | 碳酸钠 | 0.8 | V2 |
③ | 白色粉末 | a | V1 |
(4)实验装置中植物油的作用是_____;表中a=_____;V1_____V2(填“﹥”、“﹤”或“=”)。
(分析并得出结论)
(5)分析上表中数据得出结论:白色粉末的成分是_____,依据是_____。