题目内容
【题目】合金是重要的金属材料。
(1)下列物品所使用的主要材料属于合金的是_____(填字母序号)。
a.青花瓷瓶 b.橡胶充气艇 c.不锈钢锅 d.铝窗
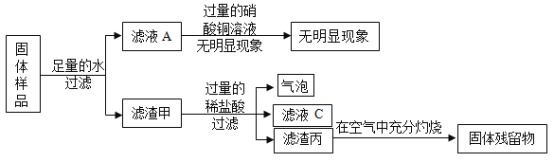
(2)黄铜是铜锌合金,黄铜渣中约含 Zn 7%、ZnO 31%、Cu 50%、CuO 5%,其余为杂质。处理黄铜渣可得到硫酸锌,其主要流程如图(杂质不溶于水、不参与反应):
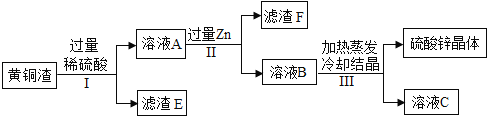
①写出步骤Ⅰ中反应的化学方程式(要求写出2种反应,反应类型相同的看作同一种反应)为_____;_____。
②步骤Ⅱ中加入过量Zn的目的是除去过量的稀硫酸和_____。
③下列说法正确的是_____
a.Ⅰ、Ⅱ、III中的操作均包含过滤
b.溶液A中ZnSO4 的质量大于CuSO4
c.溶液C中溶质的质量分数小于溶液B
④你认为滤渣E和F应该如何处理:_____。
【答案】cd ![]() (或
(或![]() )
) ![]() CuSO4 a b 回收,用于提取金属铜
CuSO4 a b 回收,用于提取金属铜
【解析】
(1)a、青花瓷瓶是用泥土烧制而成的,属于无机非金属材料,不符合题意;
b、橡胶充气艇是用合成橡胶制成的,合成橡胶属于三大合成材料之一,不符合题意;
c、不锈钢锅是用不锈钢制成的,不锈钢是铁的合金,符合题意;
d、铝窗是用铝合金制成的,铝合金是铝的合金,符合题意。
故选cd;
(2)①因为黄铜渣中含 Zn、ZnO、Cu、CuO,锌能与稀硫酸反应生成硫酸锌和氢气,该反应的化学方程式为:![]() ,该反应符合“一种单质与一种化合物反应生成另一种单质和另一种化合物”的反应,属于置换反应;氧化锌能与稀硫酸反应生成硫酸锌和水,该反应的化学方程式为:
,该反应符合“一种单质与一种化合物反应生成另一种单质和另一种化合物”的反应,属于置换反应;氧化锌能与稀硫酸反应生成硫酸锌和水,该反应的化学方程式为:![]() ,该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应;氧化铜能与稀硫酸反应生成硫酸铜和水,该反应的化学方程式为:
,该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应;氧化铜能与稀硫酸反应生成硫酸铜和水,该反应的化学方程式为:![]() ,该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应,故步骤Ⅰ中的两种反应为:
,该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应,故步骤Ⅰ中的两种反应为:![]() 、
、![]() (或
(或![]() );
);
②步骤Ⅱ中加入过量Zn,锌能与过量的稀硫酸反应生成硫酸锌和氢气,同时锌能与反应生成的硫酸铜反应生成硫酸锌和铜,故步骤Ⅱ中加入过量Zn的目的是除去过量的稀硫酸和操作Ⅰ生成的CuSO4;
③a、由图可知,操作Ⅰ过滤后得铜,操作Ⅱ过滤是除去锌,操作Ⅲ过滤是去除结晶得到的硫酸锌晶体,故Ⅰ、Ⅱ、III中的操作均包含过滤,符合题意;
b、因氧化锌的质量大于氧化铜,另外锌也能和硫酸反应生成硫酸锌,而铜和硫酸不反应,故溶液A中硫酸锌的质量大于硫酸铜,符合题意;
c、溶液B是硫酸锌的不饱和溶液,蒸发结晶后析出硫酸锌晶体,冷却至室温得到的溶液C是硫酸锌的饱和溶液,其溶质质量分数大于溶液B,不符合题意;
故选ab;
④滤渣E和F中都含有铜,所以应回收,用于提取金属铜,故填:回收、用于提取铜。

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案