题目内容
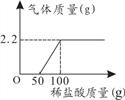
【题目】现有一瓶敞口放置在空气中的NaOH固体,欲知其组成成分,取样品9.3克向其中逐渐加入一定质量分数的稀盐酸,产生气体的质量与加入稀盐酸质量关系如图所示,试回答:
(1)产生二氧化碳气体的质量为_______克。
(2)所用稀盐酸溶质质量分数为___________。
(3)求样品中氢氧化钠的质量分数为___________。(精确到0.1%)
【答案】 2.2 7.3% 43.0%
【解析】本题考查了根据化学反应方程式的计算,认真审题,弄清反应过程,分析出盐酸与氢氧化钠反应的数据和盐酸与碳酸钠反应的数据是解题的基础。
(1)根据关系图可知,产生二氧化碳气体的质量为2.2克;
(2)根据关系图可知,氢氧化钠固体已部分变质,其组成成分是氢氧化钠与碳酸钠混合物,向样品加入盐酸,碳酸钠与盐酸反应产生的二氧化碳会被氢氧化钠吸收,等氢氧化钠完全反应后,才能放出气体,所以氢氧化钠消耗的盐酸质量为50g,碳酸钠消耗的盐酸质量=(100g-50g)=50g;设生成2.2g的二氧化碳需碳酸钠的质量为x,需盐酸中的溶质的质量为y。
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 44
x y 2.2g
![]() y=3.65g
y=3.65g
稀盐酸溶质质量分数=![]() ×100%=7.3%;
×100%=7.3%;
(3) ![]() x=5.3g
x=5.3g
样品中含有氢氧化钠质量为:9.3g-5.3g=4g,氢氧化钠的质量分数=![]() ×100%=43%。答:(1)产生二氧化碳气体的质量为2.2克。
×100%=43%。答:(1)产生二氧化碳气体的质量为2.2克。
(2)所用稀盐酸溶质质量分数为7.3%。
(3)样品中氢氧化钠的质量分数为43%。

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目