题目内容
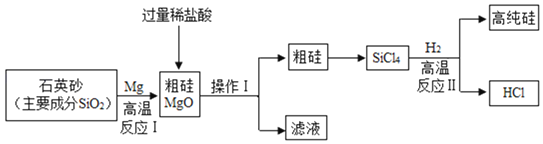
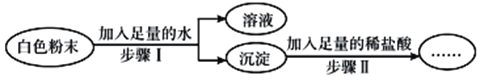
【题目】一包固体粉末可能含有镁粉、碳粉、氧化铜、氢氧化钠中的一种或几种。为探究该固体粉末的组成,某化学兴趣小组进行了如下图所示实验,下列选项错误的是![]()
![]()
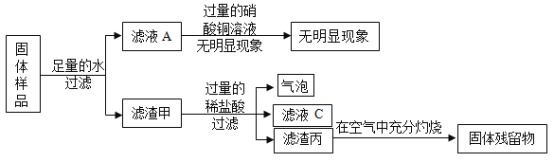
A. 向滤液A中加入无色酚酞,观察颜色变化,也可以判断其中是否含有NaOH
B. 加入稀盐酸后产生的气泡是氢气
C. 滤液C中一定含有HCl、![]() 和
和![]()
D. 原固体粉末中一定含有Mg、CuO,可能含有碳粉
【答案】C
【解析】
A、由于氢氧化钠呈碱性,能使酚酞试液变红,故向滤液A中加入无色酚酞,观察颜色变化,也可以判断其中是否含有NaOH,此选项正确;
B、镁粉、碳粉、氧化铜是难溶于水的固体物质,镁粉、碳粉、氧化铜中只有镁粉能与稀盐酸反应产生气体,所以加入稀盐酸后产生的气泡是氢气,此选项正确;
C、滤渣甲中加入盐酸产生气泡,故含有镁,镁与盐酸的反应是:Mg+2HCl== MgCl2+H2↑, 滤渣丙在空气中加热得到固体残留物,故滤渣丙中含有铜,Mg+CuCl2 ==Cu+MgCl2,所以滤液C中含有生成的氯化镁,过量的稀盐酸,不一定含有氯化铜,此选项错误;
D、原固体粉末中一定含有Mg、CuO,可能含有碳粉,此选项正确。故选C。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案【题目】小明同学欲通过实验证明“二氧化锰是氯酸钾受热分解的催化剂”这一命题,
(设计与实验)请你帮小明同学填写表中未填完的空格:
实验操作 | 实验现象 | 实验结论或总结 | ||
各步骤结论 | 总结 | |||
实验一 | 将氯酸钾加热至融化,伸入带火星的木条. | 木条复燃 | 氯酸钾受热要分解产生氧气,但是①_____. 反应的文字表达式为:②_____. | 二氧化锰是氯酸钾受热分解的催化剂 |
实验二 | 加热二氧化锰,伸入带火星的木条. | 木条不复燃 | 二氧化锰受热不产生氧气. | |
实验三 | ③_____ | 木条迅速复 燃 | 二氧化锰能加快氯酸钾的分解 | |
(交流与讨论)
(1)在小明的实验探究中,实验一和实验二的作用是_____.
(2)小英同学认为仅由上述实验还不能完全得出表内“总结”,她补充设计了两个探究实验,最终通过实验,最终完成了对“命题”的实验证明:
第一方面的实验操作中包含了两次称量,其目的是:_____;
第二方面的实验是要_____.