题目内容
(8分)小明在老师的指导下测一瓶稀盐酸的溶质质量分数,具体步骤如下:
步骤一:配制溶质质量分数为1%的氢氧化钠溶液.
步骤二:向20克待测稀盐酸中逐滴滴入上述氢氧化钠溶液,并使用pH计记录溶液的pH变化情况,绘制图像如下图。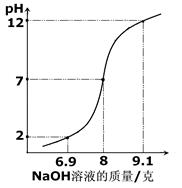
(1)在步骤一中需要用到的玻璃仪器有 。(写出两种)
(2)请结合右图,计算该稀盐酸的溶质质量分数.(结果精确到0.01%)
(3)在往稀盐酸中逐渐滴入氢氧化钠溶液的过程中,当溶液的pH达到2时,溶液中的溶质有 。(用化学式表示)
(1)玻璃棒、烧杯、量筒、胶头滴管(答出两种即可)
(2)0.37%
(3)NaCl HCl
解析试题分析:溶液配制过程中需要用到的玻璃仪器有玻璃棒、烧杯、量筒、胶头滴管,由图可知,等氢氧化钠的质量为8g时,pH等于7,即稀盐酸和氢氧化钠恰好完全反应,所以可以根据化学方程式进行计算设与20克待测盐酸完全反应消耗的氢氧化钠质量为X。
NaOH + HCl = NaCl + H2O
40 36.5
8克×1% X
40/8克×1%=36.5/X X=0.073g
盐酸的溶质质量分数为(0.073克/20克)×100%=0.37%
当溶液的pH达到2时,溶液是酸性的,所以此时溶液中一定有稀盐酸,当然还有反应生成的氯化钠。
考点:根据化学方程式进行计算,溶液成分的分析

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案
相关题目
生活处处有化学,现有以下常见的物质:
| A.生石灰 | B.盐酸 | C.熟石灰 | D.活性炭 |
(1)少量存在于人的胃液中,能帮助消化的是______;
(2)可作食品干燥剂的是_______;
(3)常用于防毒面具的是_______;
(4)改良酸性土壤的是 ;