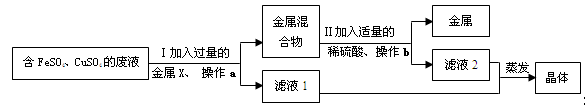
题目内容
(3分)用3个圆圈分别表示C(锌)、D(氧化铁)、E(氢氧化钡溶液)三种物质,用两圆相切表示两种物质可以发生反应,请回答下列问题:
(1)将C、D、E三个圆画到图中A、B周围适当的位置,并在圆圈中
标出三种物质的化学式;
(2)写出E发生反应的化学方程式:___________________________;
(3)写出A与B反应的现象___________________________________。
(1)如图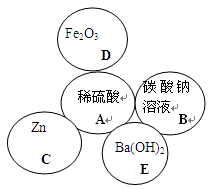
(2)Ba(OH)2 + H2SO4 = BaSO4↓ + 2H2O Ba(OH)2 + Na2CO3 = BaCO3↓+ 2NaOH
(3)(无色)溶液中有气泡产生
解析试题分析:根据酸碱盐的化学通性,可以确定各物质的位置,氢氧化钡既能和稀硫酸反应,也能和碳酸钠溶液反应,所以和A、B相切,锌和氧化铁只能和酸反应,所以只能和A相切;E发生反应的化学方程式为:Ba(OH)2 + H2SO4 = BaSO4↓ + 2H2O Ba(OH)2 + Na2CO3 = BaCO3↓+ 2NaOH;写出A与B反应的现象:有气泡冒出。
考点:物质的推断;酸碱盐的化学性质

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案将V1mL3.65% HCl溶液逐滴滴入盛有V2mL未知浓度的
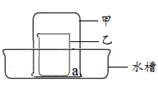
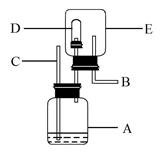
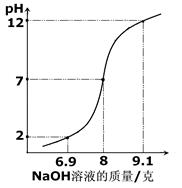
NaOH溶液的烧杯中(图1),测量并记录溶液的pH变化(图2)和
温度变化(图3)。(实验中始终保持 V1+V2=50.0mL且各种溶液密度
均为1.0g/mL)。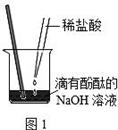
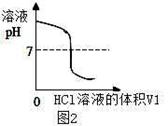
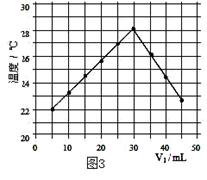
(1)图2中V1="0" mL时,图1中烧杯内溶液的颜色显 色;
(2)实验中发生反应的化学方程式为 ;
(3)图2中的pH=7时,此时滴入的HCl溶液的体积V1= mL;
(4)通过该实验给出的判断,其中正确的是 ;
| A.进行该实验时环境温度为22℃ |
| B.该实验表明化学能可转化为热能 |
| C.该实验表明有水生成的反应都是放热反应 |
| D.溶液由碱性转变为中性,再转变为酸性且酸性不断减弱 |
 丙+丁
丙+丁