题目内容
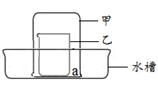
(11分)下图所示的“盆栽”中,由不同物质组成的“果子”通过短线与花盆“X”相连接(“ ”表示物质间能相互反应)。回答下列问题:
⑴ 已知甲、乙、丙均为非金属单质。
若X是氧气,通常状况下,甲、乙为固体,丙为气体。
① 物质丙的化学式为___________ ;
② 甲与X反应的化学方程式为 。
⑵ 已知甲、乙、丙均为不同类别的化合物。
① 若甲是碳酸钠,丙是能使X溶液变浑浊的气体。则物质乙的化学式是___________;
写出甲与X反应的化学方程式______________________________。
② 若X是碳酸钠,则X与下列物质在一定条件下反应关系成立的有 (填标号)。
A.X 酸 B.X 碱 C.X 盐
(1) ① H2(合理即可)(1分) ② C+O2 CO2(合理即可)(3分)
CO2(合理即可)(3分)
(2)①H2SO4(合理即可)(1分) Ca(OH)2+Na2CO3==CaCO3↓+2NaOH(合理即可)(3分)
② ABC(3分)
解析试题分析:(1)氧气的化学性质比较活泼能和许多物质发生反应,如金属、非金属、其他的复杂物质;能和氧气反应的气体单质,为氢气;甲为非金属单质,则可以为碳、硫、磷。(2)若甲为碳酸钠,丙为能使X变浑浊的气体,则丙为二氧化碳气体,X为氢氧化钙溶液,根据碱的通性,甲、乙、丙为不同类别的化合物,则乙只能为酸类物质,所以为H2SO4或HCl,甲与X反应的方程式为:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH,若X为碳酸钠,则盐类物质,根据盐的化学通性可知:盐可以和金属、酸、碱、盐反应,故选ABC。
考点:氧气的化学性质、酸碱盐的化学通性、复分解反应

将V1mL3.65% HCl溶液逐滴滴入盛有V2mL未知浓度的
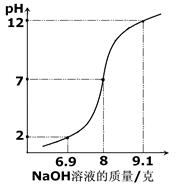
NaOH溶液的烧杯中(图1),测量并记录溶液的pH变化(图2)和
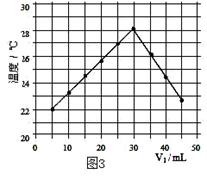
温度变化(图3)。(实验中始终保持 V1+V2=50.0mL且各种溶液密度
均为1.0g/mL)。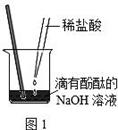
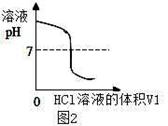
(1)图2中V1="0" mL时,图1中烧杯内溶液的颜色显 色;
(2)实验中发生反应的化学方程式为 ;
(3)图2中的pH=7时,此时滴入的HCl溶液的体积V1= mL;
(4)通过该实验给出的判断,其中正确的是 ;
| A.进行该实验时环境温度为22℃ |
| B.该实验表明化学能可转化为热能 |
| C.该实验表明有水生成的反应都是放热反应 |
| D.溶液由碱性转变为中性,再转变为酸性且酸性不断减弱 |