题目内容
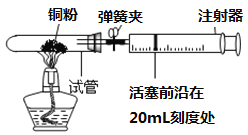
【题目】取20g碳酸钠和碳酸氢钠的固体混合物,加热至不再产生气体2NaHCO3![]() Na2CO3+H2O+CO2↑),使生成的水完全被浓硫酸吸收,测得加热时间和浓硫酸质量增加的关系如表:
Na2CO3+H2O+CO2↑),使生成的水完全被浓硫酸吸收,测得加热时间和浓硫酸质量增加的关系如表:
时间 | 0分钟 | 1分钟 | 2分钟 | 3分钟 |
仪器和浓硫酸的质量总和(g) | 150 | 150.9 | 151.8 | 151.8 |
(1)当完全反应后,生成水的质量为_____g。
(2)计算混合物中碳酸氢钠的质量分数________。(要求写出计算过程)
(3)将上述混合物完全分解后的固体溶解于186.2g 水中,待固体完全溶解后所得溶液中溶质的质量分数为_____。
【答案】1.884%。6.9%。
【解析】
解:(1)由表格可知生成水的质量为151.8g-150g=1.8g;
(2)设样品中碳酸氢钠的质量为x,生成的碳酸钠的质量为y,
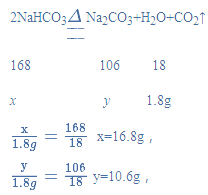
样品中碳酸氢钠的质量分数为:![]() ×100%=84%;
×100%=84%;
(3)所得溶液中溶质的质量分数为![]() ×100%=6.9%。
×100%=6.9%。

 英才计划同步课时高效训练系列答案
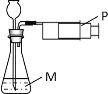
英才计划同步课时高效训练系列答案【题目】人教版化学教材第三单元有一探究实验“分子的运动”,该实验需要用到一种化学药品:浓氨水,但实验室没有该药品。于是化学老师决定用加热氯化铵和氢氧化钙固体混合物的方法制取一种密度比空气小的气体:氨气,然后用制得的氨气常温下与水反应制得浓氨水,请回答下列问题:
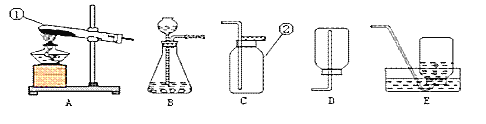
(1)写出指定仪器的名称:② ______________________。
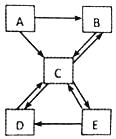
(2)老师选择制取氨气的发生装置是(填序号,下同)_______,收集装置是_____
(3)同学们认为用制取氨气的装置也可以用于实验室制取氧气,则他们选择的药品是___,
该反应的原理是(写文字表达式)_____,若同学们想收集一瓶纯净的氧气,则选择的装置是__________
(4)小亮对铁丝在氧气中燃烧为什么会火星四射进行探究.下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为![]() )放入氧气中燃烧时的实验现象的记录.请你分析回答:
)放入氧气中燃烧时的实验现象的记录.请你分析回答:
物质 | 镁条 | 含碳 | 含碳 | 含碳 |
燃烧时 的现象 | 剧烈燃烧,发出 耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 未填 |
①表中“未填”部分的内容应为________;
②通过以上探究,你认为铁丝燃烧产生火星四射现象的原因可能是________.
③实验结束后,小亮同学发现集气瓶底破裂,则可能的原因是_______