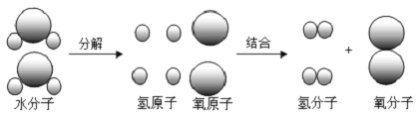
题目内容
【题目】为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为40mL的试管作反应容器,将过量的铜粉放入试管,用橡皮塞塞紧试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如下图的实验装置。假设此实验能够按照小华的设想正常进行,且铜粉所占体积与导管内的气体体积忽略不计,请回答下列问题:
资料:铜在加热条件下只能与氧气反应,而镁在加热条件下不仅与氧气反应,还能与氮气、二氧化碳等起反应。
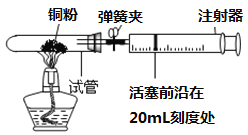
(1)实验前,打开弹簧夹,将注射器活塞前沿从20mL刻度处推至15mL刻度处,然后松开手,若活塞仍能返回至20mL刻度处,则说明_______________________________;
(2)若不使用弹簧夹,用酒精灯加热铜粉,充分反应直至燃烧结束,试管冷却。可观察到的现象为_______________________,铜粉充分反应的文字表达式:_____________;
(3)不能用木炭替代铜粉的原因:____________;不用镁替代铜粉的原因:_______________;
(4)该装置相对于书本提供的装置的优点:_______________;
(5)如果完全冷却后,实验测得结果小于1/5。原因:____________。
【答案】气密性良好;活塞前沿在40mL刻度处;铜+氧气![]() 氧化铜;生成物是气体,压强几乎不变;镁不仅与氧气反应,还能与氮气、二氧化碳等反应;气密性更好(结果更精确)或无污染(答案合理的均可);铜粉不足。
氧化铜;生成物是气体,压强几乎不变;镁不仅与氧气反应,还能与氮气、二氧化碳等反应;气密性更好(结果更精确)或无污染(答案合理的均可);铜粉不足。
【解析】
(1)根据装置气密性检查方法分析解答;
(2)根据氧气约占空气体积的五分之一分析解答;根据铜与氧气在加热的条件下生成氧化铜解答;
(3)根据生成物的状态及镁能够与空气中的多种组成成分反应分析解答;
(4)根据该装置的特点分析解答;
(5)根据实验注意事项分析解答。
(1)打开弹簧夹,将注射器活塞前沿从20mL刻度处推至15mL刻度处,然后松开手,若活塞仍能返回至20mL刻度处,则说明气密性良好;
(2)若不使用弹簧夹,用酒精灯加热铜粉,充分反应直至燃烧结束,试管冷却。可观察到的现象为活塞前沿在[60mL-(40mL+60mL)×![]() ]=40mL刻度处,铜粉充分反应的文字表达式:铜+氧气
]=40mL刻度处,铜粉充分反应的文字表达式:铜+氧气![]() 氧化铜;
氧化铜;
(3)不能用木炭替代铜粉的原因:生成物是气体,压强几乎不变;不用镁替代铜粉的原因:镁不仅与氧气反应,还能与氮气、二氧化碳等反应;
(4)该实验中药品在密闭的装置内反应,故该装置相对于书本提供的装置的优点:无污染(答案合理的均可);
(5)如果完全冷却后,实验测得结果小于1/5。原因:铜粉不足。

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案【题目】取20g碳酸钠和碳酸氢钠的固体混合物,加热至不再产生气体2NaHCO3![]() Na2CO3+H2O+CO2↑),使生成的水完全被浓硫酸吸收,测得加热时间和浓硫酸质量增加的关系如表:
Na2CO3+H2O+CO2↑),使生成的水完全被浓硫酸吸收,测得加热时间和浓硫酸质量增加的关系如表:
时间 | 0分钟 | 1分钟 | 2分钟 | 3分钟 |
仪器和浓硫酸的质量总和(g) | 150 | 150.9 | 151.8 | 151.8 |
(1)当完全反应后,生成水的质量为_____g。
(2)计算混合物中碳酸氢钠的质量分数________。(要求写出计算过程)
(3)将上述混合物完全分解后的固体溶解于186.2g 水中,待固体完全溶解后所得溶液中溶质的质量分数为_____。