题目内容
(10分)过氧化钙(CaO2)是一种对环境友好的多功能无机化合物,通常有两种制备方法。已知:温度过高过氧化钙会分解生成氧化物和氧气。
方法1:由Ca(OH)2为原料最终制得,其制备流程如下:
方法2:由鸡蛋壳(含CaCO3高达90%)为原料最终反应制得,其制备流程如下: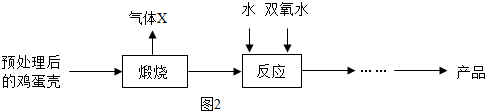
(1)方法1中搅拌的目的是 。请将搅拌过程中发生反应的化学方程式补充完整:
CaCl2 + H2O2 + 2NH3·H2O + 6 = CaO2·8H2O↓+ 2NH4Cl。制备过程中除水外可循环使用的物质是 (填化学式);
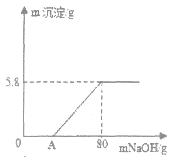
(2)方法2中气体X是 ,实验室常用 溶液来吸收。煅烧后的反应时化合反应,也能生成CaO2·8H2O,反应的化学方程式为 。该反应需控制温度在0 ~ 2℃,可将反应器放置在 中,获得CaO2产品中主要含有的固体杂质是 (填化学式);
(3)这两种制法均要求在低温下进行(除煅烧外),温度过高除了防止氨水挥发外,还能 ;
(4)“绿色化学”一般是指反应物的原子全部转化为期望的最终产物,则上述两种方法中生成CaO2·8H2O的反应符合“绿色化学”的是 (填“方法1”或“方法2”)。
(1)使反应充分,提高原料利用率;H2O;NH4Cl;(2)CO2,NaOH,Ca(OH)2+H2O2+7H2O=CaO2?8H2O,冰水中,Ca(OH)2;(3)使CaO2分解;(4)方法2.
解析试题分析:(1)方法1中搅拌的目的是:使反应充分,提高原料利用率,因为搅拌可使原料充分混合;依据质量守恒定律可知,化学反应前后原子个数不变,所以化学方程式中缺少的是H2O;NH4Cl既出现在了反应物中,也出现在了生成物中,所以制备过程中除水外可循环使用的物质是NH4Cl;
(2)鸡蛋壳的主要成分是CaCO3,CaCO3在高温的条件下生成CaO和CO2,所以X是CO2;在实验室常用氢氧化钠溶液来吸收二氧化碳,用澄清石灰水来检验二氧化碳;氧化钙与水反应生成氢氧化钙,氢氧化钙和双氧水、水反应生成过氧化钙晶体,则化学方程式为:Ca(OH)2+H2O2+7H2O=CaO2?8H2O;因为反应需控制温度在0~2℃,而冰水混合物的温度是0℃,所以可将反应器放置在冰水中;在化学反应中,反应物不一定会全部转化为生成物,而该反应中只有氢氧化钙是固体反应物,所以获得的CaO2产品中主要含有的固体杂质是Ca(OH)2;
(3)已知:温度过高过氧化钙会分解生成氧化物和氧气,所以温度过高会造成氨水挥发外,还能使CaO2分解;
(4)“绿色化学”一般是指反应物的原子全部转化为期望的最终产物,方法1中有副产物氯化铵,方法2中没有副产物,所以上述两种方法中生成CaO2?8H2O的反应符合“绿色化学”的是:方法2。
考点:碳及其化合物、碱的化学性质、质量守恒定律及其应用、书写化学方程式

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如下图所示。要求同学们进行探究:确认这瓶溶液到底是什么溶液?
【提出猜想】王老师提示:这瓶无色溶液只能是下了四种溶液中的一种:①硫酸镁溶液、②硫酸钠溶液、③硫酸溶液、④硫酸铵溶液
【查阅资料】(1)常温下,相关物质的溶解度如下:
| 物质 | MgSO4 | Na2SO4 | (NH4)2SO4 | H2SO4 |
| 溶解度 | 35.1g | 19.5g | 75.4g | 与水任意比互溶 |
(2)(NH4)2SO4的水溶液显酸性
【实验探究】(1)通过查阅资料,小明同学认为猜想 (填序号)不成立,原因是 。
(2)为确定其它几种猜想是否正确,小明同学继续进行探究:
| 实验操作 | 实验现象 | 实验结论 |
| ①取该溶液少许于试管中,向其中滴加几滴 溶液 | 溶液中有白色沉淀生成 | 猜想①成立 |
| ②用玻璃棒蘸取少许原溶液滴在pH试纸水,并跟比色卡对照 | 溶液pH小于7 | 猜想③成立 |
小雅同学认为小明实验操作②的结论不正确,她的理由是 ;
(3)请你设计实验方案,确认该溶液是硫酸铵溶液并完成实验报告:
| 实验操作 | 实验现象 | 实验结论 |
| 取该溶液少许于试管中, | | 猜想④成立,该反应的化学方程式为 |
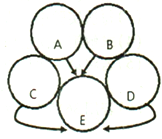
某同学用下图装置验证某混合气体中一定含有水蒸气、二氧化碳和一氧化碳三种气体。
|
 (1)该同学验证三种气体一定存在。实验进行时,若要气体从左向右流动,则这几种仪器的连接顺序应是:混合气体→( ) →( ) →( )→ E → D→( ) →( )(填A、B、C或E,可重复使用);
(1)该同学验证三种气体一定存在。实验进行时,若要气体从左向右流动,则这几种仪器的连接顺序应是:混合气体→( ) →( ) →( )→ E → D→( ) →( )(填A、B、C或E,可重复使用);(2)混合气体通过A装置发生反应的化学方程式为______________________________