题目内容
把44g刚烘干的木碳粉和氧化铜粉末放在试管中加热,完全反应后,冷却,称得剩余固体33g.实验后把该剩余固体放在空气中灼烧没有观察到物质的燃烧现象.求:
(1)根据质量守恒定律计算可制得二氧化碳多少克?
(2)剩余固体含有什么物质?各多少克?
(1)根据质量守恒定律计算可制得二氧化碳多少克?
(2)剩余固体含有什么物质?各多少克?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据固体减少的质量就是生成二氧化碳的质量解答;
(2)根据化学方程式,通过二氧化碳的质量计算出氧化铜的质量,然后分析判断.
(2)根据化学方程式,通过二氧化碳的质量计算出氧化铜的质量,然后分析判断.
解答:解:
(1)根据质量守恒定律生成CO2的质量为:44g-33g═11g
(2)因木炭粉已完全反应了,剩余的固体中肯定有Cu,可能还有CuO
设:生成Cu的质量为x
C+2CuO
2Cu+CO2↑
2×64 44
x 11g
=
x=32g
剩余CuO的质量为:33g-32g=1g
答案:
(1)根据质量守恒定律计算可制得二氧化碳为11克
(2)剩余固体含有铜32g,氧化铜1g
(1)根据质量守恒定律生成CO2的质量为:44g-33g═11g
(2)因木炭粉已完全反应了,剩余的固体中肯定有Cu,可能还有CuO
设:生成Cu的质量为x
C+2CuO
| ||
2×64 44
x 11g
| 2×64 |
| 44 |
| x |
| 11g |
x=32g
剩余CuO的质量为:33g-32g=1g
答案:
(1)根据质量守恒定律计算可制得二氧化碳为11克
(2)剩余固体含有铜32g,氧化铜1g
点评:本题主要考查学生运用化学方程式进行计算的能力,根据化学方程式计算时一定要注意格式和计算的准确性.

练习册系列答案
相关题目
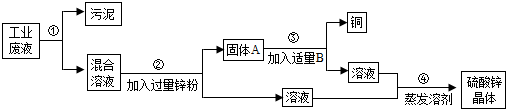
 某校研究性学习小组进行了一个有趣的实验探究:
某校研究性学习小组进行了一个有趣的实验探究: