题目内容
某化工厂排放的废液中含有大量的硫酸锌和硫酸铜,化学兴趣小组的同学根据所学知识设计了一个方案,用来回收金属铜并得到硫酸锌晶体,主要过程如图所示:
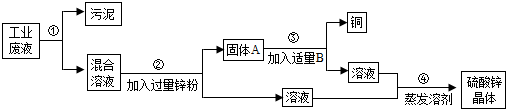
请回答下列问题:
(1)步骤②中分离物质的方法是 .
(2)固体A的成分是 ,B的名称是 .
(3)步骤②中发生反应的化学方程式为 ,该反应属于基本反应类型中的 反应.
(4)步骤③中加入“适量B”的具体操作是: .
(5)步骤④中得到硫酸锌晶体的方法是 .

请回答下列问题:
(1)步骤②中分离物质的方法是
(2)固体A的成分是
(3)步骤②中发生反应的化学方程式为
(4)步骤③中加入“适量B”的具体操作是:
(5)步骤④中得到硫酸锌晶体的方法是
考点:金属的化学性质,过滤的原理、方法及其应用,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:一般的除杂质题必须同时满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应②反应时不能加入新的杂质.根据题目给出的流程图和信息:固体与液体分开的方法叫过滤;硫酸锌和硫酸铜的混合液中加入过量的锌粉,锌与硫酸铜反应生成硫酸锌和铜,过滤后固体A是铜和锌的混合物,滤液是硫酸锌溶液;铜和锌的混合物中加入适量的稀硫酸,铜不反应,锌与硫酸反应生成硫酸锌和氢气,过滤得到铜,滤液是硫酸锌;然后把硫酸锌溶液蒸发结晶得到硫酸锌晶体;据此逐项分析.
解答:解:(1)固体与液体分开的方法叫过滤,故答案为:过滤;
(2)硫酸锌和硫酸铜的混合液中加入过量的锌粉,锌与硫酸铜反应生成硫酸锌和铜,过滤后固体A是铜和锌的混合物,铜和锌的混合物中加入适量的稀硫酸,铜不反应,锌与硫酸反应生成硫酸锌和氢气,过滤得到铜,滤液是硫酸锌溶液;故答案为:锌和铜;稀硫酸;
(3)锌与硫酸铜反应生成硫酸锌和铜,该反应是单质和化合物的反应产生新的单质和化合物,属于置换反应;故答案为:Zn+CuSO4═Cu+ZnSO4;置换;
(4)铜和锌的混合物中加入适量的稀硫酸,铜不反应,滴加稀硫酸至不再产生气体为止,说明锌被完全反应,锌与硫酸反应生成硫酸锌和氢气,过滤得到铜,滤液是硫酸锌;故答案为:滴加稀硫酸至不再产生气体为止;
(5)步骤④中从硫酸锌溶液得到硫酸锌晶体可以通过蒸发溶剂;故答案为:蒸发溶剂.
(2)硫酸锌和硫酸铜的混合液中加入过量的锌粉,锌与硫酸铜反应生成硫酸锌和铜,过滤后固体A是铜和锌的混合物,铜和锌的混合物中加入适量的稀硫酸,铜不反应,锌与硫酸反应生成硫酸锌和氢气,过滤得到铜,滤液是硫酸锌溶液;故答案为:锌和铜;稀硫酸;
(3)锌与硫酸铜反应生成硫酸锌和铜,该反应是单质和化合物的反应产生新的单质和化合物,属于置换反应;故答案为:Zn+CuSO4═Cu+ZnSO4;置换;
(4)铜和锌的混合物中加入适量的稀硫酸,铜不反应,滴加稀硫酸至不再产生气体为止,说明锌被完全反应,锌与硫酸反应生成硫酸锌和氢气,过滤得到铜,滤液是硫酸锌;故答案为:滴加稀硫酸至不再产生气体为止;
(5)步骤④中从硫酸锌溶液得到硫酸锌晶体可以通过蒸发溶剂;故答案为:蒸发溶剂.
点评:本考点属于物质的除杂或净化的探究,还考查了化学方程式的书写,是中考的一个难点,也是学生经常出错的题型.根据物质的溶解性和除杂质的条件,要认真分析,综合把握.还要加强记忆除去常用离子的方法和物质的溶解性,从而突破难点.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
如图是三种微粒的结构示意图,有关他们的说法正确的是( )

| A、它们都是原子 |
| B、它们的相对原子质量相同 |
| C、它们的最外层电子数相同 |
| D、它们属于同种元素的微粒 |
下列符号中,既表示一个原子,又表示一种元素,还表示一种物质的是( )
| A、2H |
| B、He |
| C、2H2 |
| D、H2O |
下列反应属于化合反应的是( )
| A、蜡烛+氧气-→水+二氧化碳 |
| B、氧化汞-→汞+氧气 |
| C、过氧化氢-→水+氧气 |
| D、氢气+氧气-→水 |

 用Ba(OH)2溶液测定某种氮肥中(NH4)2SO4的质量分数(杂质溶于水,但不参加反应).实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入Ba(OH)2溶液,生成气体及沉淀质量与加入Ba(OH)2溶液的质量关系如下所示:
用Ba(OH)2溶液测定某种氮肥中(NH4)2SO4的质量分数(杂质溶于水,但不参加反应).实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入Ba(OH)2溶液,生成气体及沉淀质量与加入Ba(OH)2溶液的质量关系如下所示: