题目内容
【题目】过氧化钙(CaO2)是一种重要的化工产品,能杀菌消毒,广泛用于果蔬保鲜、 空气净化、污水处理等方面。某兴趣小组同学对其进行了有关探宄。
(查阅资料)
(1)过氧化钙是白色、无毒、难溶于水的白色粉末。
(2)![]() 。
。
(3)![]() ;二氧化锰与稀盐酸不反应。
;二氧化锰与稀盐酸不反应。
(探宄1)验证过氧化钙受热分解的产物。
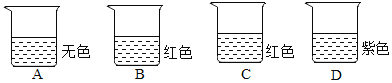
(1)取少量纯净的过氧化钙放入试管中充分加热,将带火星的木条伸入试管,可观察到带火星的木条_______。
(2)待(1)中试管冷却,取管中少量固体加水充分搅拌,静置,向上层清液中滴加几滴酚酞试液,可观察到溶液变成_________色。
(探宄2)测定产品中过氧化钙的质量分数(假设过氧化钙产品中只含有氧化钙杂质)。
(实验装置)
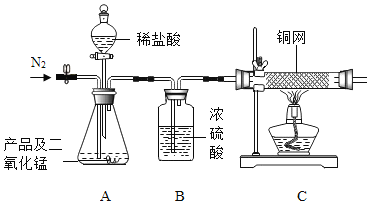
(实验步骤)
①连好装置并检查装置的气密性,在锥形瓶中放入4g该产品;②实验前称量C中铜网的质量;③先缓慢通入氮气,一段时间后加热铜网至红热;再缓慢滴入过量稀盐酸,直至A中样品完全反应;④继续缓慢通入氮气,一段时间后停止加热,待C中铜网冷却后,停止 通入氮气;⑤再次称量C中铜网的质量,发现比反应前増重0.8g。
(实验结论)
(1)A中二氧化锰的作用是____________________。
(2)C中铜网发生反应的化学方程式为______________。
(3)该产品中过氧化钙的质量分数为___________。
(拓展提升)若A中样品完全反应后,立即停止通氮气并熄灭酒精灯,待C中铜网冷却后称量其质量。你认为该操作对测定产品中过氧化钙的质量分数是否有影响?_____________。(选填“是”或“否”,并说明理由)。
【答案】复燃 红 催化过氧化钙和水生成的过氧化氢的分解 ![]() 90% 有,A中样品完全反应后,立即停止通氮气并熄灭酒精灯,将导致部分生成的 氧气残留于A装置中,以及由于温度不够高,部分氧气未能与铜网反应,进而导致铜网増 重偏小。该结果将最终导致CaO2质量分数偏低。
90% 有,A中样品完全反应后,立即停止通氮气并熄灭酒精灯,将导致部分生成的 氧气残留于A装置中,以及由于温度不够高,部分氧气未能与铜网反应,进而导致铜网増 重偏小。该结果将最终导致CaO2质量分数偏低。
【解析】
[探究1](1)由由查阅资料可知,过氧化钙加热产生氧气,氧气具有助燃性,可以使带火星的木条复燃,故填写:复燃;
(2)由查阅资料可知,过氧化钙加热除产生氧气,还产生氧化钙,氧化钙与水反应生成氢氧化钙,氢氧化钙溶液显碱性,可以使无色酚酞变为红色,故填写:红;
[实验结论](1)由图可知,装置A是过氧化钙和二氧化锰中滴加稀盐酸,稀盐酸与过氧化钙反应产生氯化钙和过氧化氢,二氧化锰可以催化过氧化氢分解产生氧气,故填写:催化过氧化钙和水生成的过氧化氢的分解;
(2)铜和氧气在加热条件下生成氧化铜,故填写:![]() ;
;
(3)CaO2质量分数的计算:铜网增重量0.8g为CaO2分解产生氧气的质量,
解:设产生0.8g氧气需要分解过氧化钙的质量为x

该产品中过氧化钙的质量分数为:![]() =90%,故填写:90%;
=90%,故填写:90%;
[拓展提升]有,A中样品完全反应后,立即停止通氮气并熄灭酒精灯,将导致部分生成的 氧气残留于A装置中,以及由于温度不够高,部分氧气未能与铜网反应,进而导致铜网増 重偏小。该结果将最终导致CaO2质量分数偏低,故填写:有,A中样品完全反应后,立即停止通氮气并熄灭酒精灯,将导致部分生成的 氧气残留于A装置中,以及由于温度不够高,部分氧气未能与铜网反应,进而导致铜网増 重偏小。该结果将最终导致CaO2质量分数偏低。

【题目】HDPE膜被广泛应用于固体废弃物填埋场、沼气池、污水处理池、水产养殖池塘、水库大坝等各种防水、防渗、防腐工程。HDPE膜具有极好的抗冲击性和防潮性,听完老师的描述后,同学们对HDPE膜的组成元素产生了浓厚的兴趣,进行了如下探究。
(提出问题)HDPE膜由什么元素组成?
(查阅资料)①HDPE膜能够燃烧,燃烧可能生成一氧化碳;
②碱石灰主要成分是氢氧化钠固体和氧化钙固体。
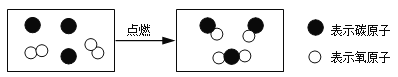
(实验探究)如图所示,先通入干燥氮气,再将4.2g的HDPE膜样品在一定质量的氧气中点燃,并将燃烧产物依次通过装置A、B、C、D(装置中每步反应均进行完全)。

(实验记录)
装置质量 | A装置总质量 | C装置总质量 |
实验前 | 100.0g | 100.0g |
实验后 | 105.4g | 113.2 |
(1)实验中观察到装置B中________可作为HDPE膜燃烧生成一氧化碳的依据。
(实验分析)
(2)装置A中浓硫酸的作用是_______
(数据处理)
(3)装置C中盛有过量的NaOH溶液,分析实验结束后装置C中溶液的溶质。请设计实验方案探究溶质成分
步骤 | 现象 | 结论 |
_____. | ____. | ____. |
(实验结论)(4)HDPE膜由________元素组成。
(反思评价)(5)若无D装置对实验结果有何影响?______。