题目内容
【题目】某研究小组对过氧化氢溶液制取氧气进行如下探究:
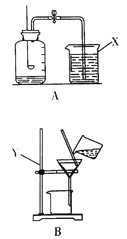
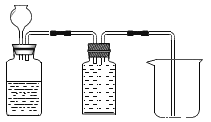
实验一:如图装置可用于多次连续进行氧气的制取和性质的实验。
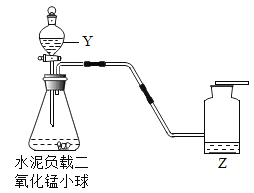
(1)仪器Y的名称是_______。
(2)该反应的化学式表达式:________,二氧化锰在反应中的作用是___。多孔水泥负载二氧化锰小球用于实验时的主要优点是_____,检验氧气已收集满的方法_________。
(3)做氧气的性质实验时,实验不同,Z的作用不同。
①铁丝燃烧。Z为水,其作用是_____。
②蜡烛燃烧。Z为______,其作用是验证蜡烛燃烧生成了二氧化碳。
实验二:探究H2O2质量分数、溶液pH、温度对反应速率的影响
(2)设计如下表实验方案:
实验序号 | H2O2质量分数/% | pH | 温度/℃ | 每分钟气泡数 |
1 | 30 | 5 | 20 | |
2 | 30 | 6 | 20 | |
3 | 30 | 11 | 20 | |
4 | 15 | 11 | 30 | |
5 | a | 11 | b |
①进行实验1~3的目的是探究________。
②a=_________;b=_________。
实验三:探究制取氧气的适宜催化剂

(3)实验方案如下:
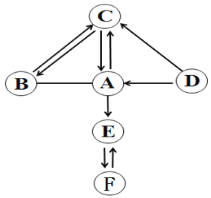
I.用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
II.取30粒含MnO2的海藻酸钠微球,采用左下图装置进行实验。改用其他三种微球,分别重复上述实验,得到右下图的锥形瓶内压强随时间变化的曲线图。
①每次实验时,海藻酸钠微球数应相同的原因_________。
②用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是____。
③从实验曲线看,催化效果较好、反应温和的催化剂是______。
【答案】分液漏斗 H2O2![]() H2O + O2 催化 增大接触面积 将带火星的木条放在瓶口 防止生成物溅落瓶底,使集气瓶炸裂 澄清石灰水 溶液pH对反应速率的影响 15 20 控制变量 反应速度太快,导致瓶内气压过大,橡皮塞被弹出 CuO
H2O + O2 催化 增大接触面积 将带火星的木条放在瓶口 防止生成物溅落瓶底,使集气瓶炸裂 澄清石灰水 溶液pH对反应速率的影响 15 20 控制变量 反应速度太快,导致瓶内气压过大,橡皮塞被弹出 CuO
【解析】
实验一:(1)通过分析入题中所指仪器的名称和作用可知,Y是分液漏斗;
(2)水泥负载二氧化锰小球用于实验时的主要优点是:增大接触面积、便于二氧化锰的回收利用;该实验中收集氧气的方法是:向上排空气法;检验氧气已收集满的方法:将带火星的木条放在瓶口;
(3))①铁丝燃烧,生成高温的四氧化三铁,Z为水,其作用是:防止溅落的熔化物炸裂瓶底;
②蜡烛燃烧,Z为澄清石灰水,其作用是验证蜡烛中含有碳元素;
实验二:①实验1~3的溶液浓度相同,温度相同,pH不同,故该实验是探究溶液的pH对反应速率的影响;
②进行实验时要注意控制变量,4、5的pH相同,需要控制过氧化氢溶液的溶质质量分数相同或是温度相同,故a可以是15;可以是20,或是a是30,b是30;
实验三:)①每次实验时,海藻酸钠微球数应相同是为了确保催化剂用量一致;
②用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,可能是因为产生气体的速率过快,导致气压过大,橡皮塞被弹出;
③从实验曲线看,二氧化锰太剧烈,氧化铁和三氧化二铬太慢,故催化效果较好、反应温和的催化剂是CuO。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案