题目内容
为测定某BaCl2溶液的溶质质量分数,现取100gBaCl2溶液,不断加入稀H2SO4,反应过程中溶液质量与加入稀H2SO4的质量关系如图所示,(反应方程式:BaCl2+H2SO4=BaSO4↓+2HCl)请回答: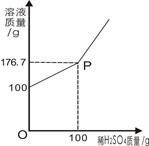
(1)P点意义_______________。
(2)反应生成BaSO4沉淀的质量为_________g。
(3)求原BaCl2溶液的溶质质量分数。
解析试题分析:①P点是硫酸和氯化钡恰好完全反应的点,②反应生成BaSO4沉淀的质量为加入100g稀硫酸后溶液少增加的质量,为100g+100g-176.7g=23.3g;
③解:设BaCl2质量为X
BaCl2+H2SO4=BaSO4 +2HCl
208 233
X 23.3g
208/X=233/23.3
解得X=20.8g
原BaCl2溶液的溶质质量分数为20.8/100g*100%=20.8%
答:原BaCl2溶液的溶质质质量分数为20.8%
考点:有关化学方程式的计算

练习册系列答案
相关题目
为测定某生理盐水的溶质质量分数,现将生理盐水样品与足量的硝酸银溶液混合,相关实验数据如下表所示(不计损耗):
| | 反应前 | 反应后 | |
| 实验 数据 | 生理盐水样品的质量 | 加入硝酸银溶液的质量 | 过滤后剩余溶液的质量 |
| 130 g | 40 g | 167.13 g | |
(1)反应后生成氯化银固体的质量为 g。
(2)请计算该生理盐水中含氯化钠的物质的量(根据化学方程式列式计算) 。
(3) 。