题目内容
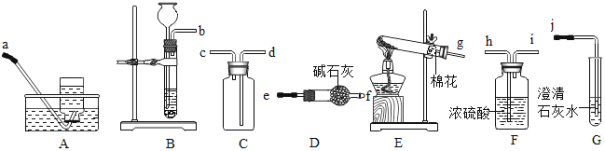
【题目】实验一:如图是实验室制取气体常用的装置,回答问题:
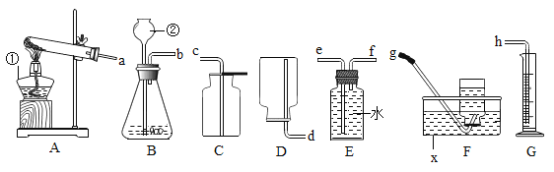
(1)写出标号仪器的名称:①___________________、②_______________________;
(2)若实验室要用同一装置制取并收集O2和CO2,最好选择____________装置组合(填标号),写出用该装置制取O2的化学方程式____________________________________________________________。
(3)实验室用锌与稀硫酸反应来制取氢气并测定氢气的体积,请从图中选择最佳的装置进行组合,整套装置的导管口连接顺序是________(填标号)
Aa→d Bb→g Cb→e→f→h Db→f→e→h
(4)氨气(NH3)是一种无色有刺激性气味的气体,密度比空气小,极易溶于水,实验室常用加热氯化铵和氢氧化钙的固体混合物制取氨气。可选用如图中____________(填标号)装置组合制取并收集氨气。若用如图装置收集,氨气应从________(填“a”或“b”)导管口进入。
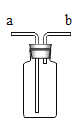
实验二:某同学将光亮的镁条放入NaHCO3饱和溶液中,镁条消失并产生大量气泡和白色固体。为确定产生的气体和白色固体的成分,该同学进行了如下的探究。
(查阅资料)①Mg(HCO3)2能溶于水;
②MgCO3、Mg(OH)2加热易分解,分别生成两种氧化物。
③碱石灰主要成分是NaOH和CaO的混合物。
(猜想假设)①白色固体可能是Mg(OH)2;
②白色固体可能是MgCO3;
③白色固体可能是__________________。
(进行实验)
(1)收集并点燃产生的气体,火焰呈淡蓝色,火焰上方罩涂有澄清石灰水的小烧杯,无明显现象,则该气体为_________。
(2)对白色固体进行实验:
实验步骤 | 现象 | 结论 |
①取洗净后的白色固体,加入足量的________ | 观察到______ | 白色固体一定含有MgCO3 |
②取一定量白色固体,充分加热至不再产生气体,将产生的气体先通入碱石灰,再通入浓硫酸,分别称量装置反应前后的质量 | 碱石灰增重,浓硫酸不变 | 白色固体一定含有_______,可能含有___。 |
(反思评价)为进一步确定可能含有的物质,对实验②如何改进,写出具体的操作方法和结论_______________。
【答案】酒精灯 长颈漏斗 BC 2H2O2![]() 2H2O + O2↑ D AD b MgCO3 和 Mg(OH)2 H2 稀盐酸 固体溶解,有气泡产生 MgCO3 Mg(OH)2 将加热后产生的气体通入浓硫酸中,称量。如果浓硫酸增重,固体中含有MgCO3 和 Mg(OH)2 ;如不增重,固体中只有MgCO3
2H2O + O2↑ D AD b MgCO3 和 Mg(OH)2 H2 稀盐酸 固体溶解,有气泡产生 MgCO3 Mg(OH)2 将加热后产生的气体通入浓硫酸中,称量。如果浓硫酸增重,固体中含有MgCO3 和 Mg(OH)2 ;如不增重,固体中只有MgCO3
【解析】
(1)实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素。
(2)根据碳酸根离子的检验、水蒸气的检验方法进行分析。
1、实验一
(1)标号仪器的名称:①酒精灯;②长颈漏斗。
(2)若实验室要用同一装置制取并收集O2和CO2,只能是固液常温型发生装置和向上排空气法收集气体,最好选择BC装置组合;写出用该装置制取O2是过氧化氢和二氧化锰制取氧气,化学方程式2H2O2![]() 2H2O + O2↑ 。
2H2O + O2↑ 。
(3)实验室用锌与稀硫酸反应来制取氢气并测定氢气的体积,发生装置是固液常温型装置B,收集装置是E,测氢气体积是G。连接顺序是b→f→e→h,故选D。
(4)氨气(NH3)是一种无色有刺激性气味的气体,密度比空气小,极易溶于水,只能用向下排空气法收集,实验室常用加热氯化铵和氢氧化钙的固体混合物制取氨气,发生装置是固体加热型。可选用如图中AD装置组合制取并收集氨气。氨气(NH3)密度比空气小,若用如图装置收集,氨气应从b导管口进入。
2、实验二
【猜想假设】
③白色固体可能是MgCO3 和 Mg(OH)2的混合物。
【进行实验】
(1)氢气点燃产生淡蓝色火焰,火焰上方罩涂有澄清石灰水的小烧杯,无明显现象,则该气体为氢气。
(2)对白色固体进行实验:
①取洗净后的白色固体,加入足量的稀盐酸;观察到固体溶解,有气泡产生,白色固体一定含有MgCO3。
②取一定量白色固体,充分加热至不再产生气体,将产生的气体先通入碱石灰,后通入浓硫酸,分别称量装置反应前后的质量,碱石灰增重,说明气体中有二氧化碳,浓硫酸不变说明可能有水蒸气, 白色固体一定含有MgCO3;可能含有Mg(OH)2。
【反思评价】
为进一步确定可能含有的物质,对实验②如何改进,写出具体的操作方法和结论:将加热后产生的气体先通入浓硫酸后通入碱石灰,称量。如果浓硫酸增重,固体中含有MgCO3 和 Mg(OH)2 ;如不增重,固体中只有MgCO3。

【题目】小红学碱的性质时做了如图两个实验,并把两个实验的滤液都倒入了一个烧杯中,结果烧杯中产生了少量气泡,最终还有白色沉淀生成。回答下列问题:
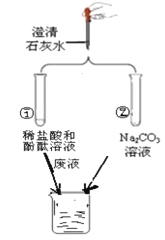
(1)实验①中酚酞溶液的作用___________________。
(2)实验②中滤液的溶质除有氢氧化钠外,还有________________(填化学式)。
(3)烧杯中产生白色沉淀物的化学方程式 ____________。
(4)小红对烧杯中的溶质的成分进行探究:小红认为除有NaCl外,还可能含有:
猜想1:还可能含有CaCl2
猜想2: 还可能含有___________,为了验证猜想1提出方案如下:
实验操作 | 实验现象 | 实验结论 |
取烧杯中的少量滤液于试管中,加入Na2CO3溶液 | _____________________ | 猜想1正确 |