题目内容
【题目】宏微结合是初中化学核心素养之一。
(1)从微观知宏观
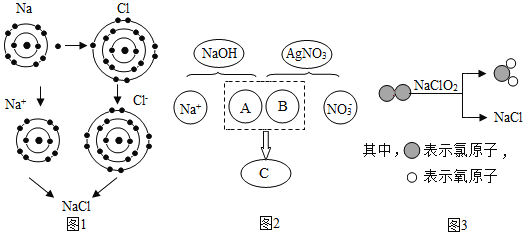
图中所示为元素周期表中部分元素的相关信息,请利用下表回答相关问题:
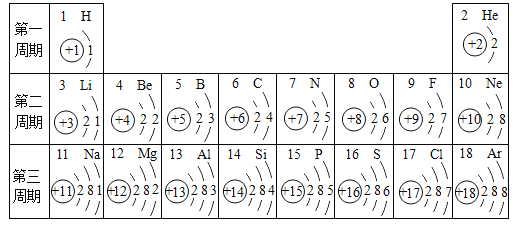
①氟元素的原子比氯元素的原子化学性质活泼的原因是_____。
②写出11号元素和16号元素形成化合物的化学式_____。
(2)从宏观知微观
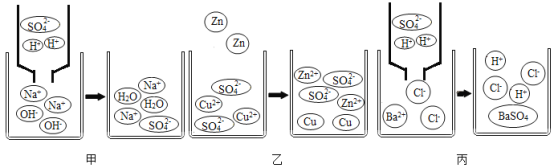
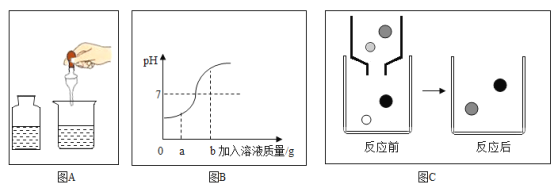
①从微粒的角度说明图甲反应的实质是_____;所示反应中,图乙参加反应的化学方程式为_____。
②H2SO4溶液能与BaCl2溶液反应产生白色沉淀,其微观变化过程如上图丙所示,参加反应的离子是_____(填离子符号)。已知FeCl3溶液能与NaOH溶液反应生成红褐色沉淀,从反应的微观实质可以推测出Fe2(SO4)3溶液可以和某溶液反应同时生成两种沉淀,写出该反应的化学方程式_____。
【答案】氟原子的电子层数少 Na2S 氢离子和氢氧根离子生成水分子 Zn + Cu SO4== ZnSO4 + Cu Ba2+、SO42- Fe 2(SO4)3+3 Ba(OH)2=3 BaSO4↓+2 Fe (OH)3↓
【解析】
(1)①原子的化学性质由原子的最外层电子数和电子层数决定,氟元素的原子比氯元素的原子化学性质活泼的原因是氟原子的电子层数少;
②化合价与一个原子得到或失去的电子数有关,得电子数等于负价的数值,失电子数等于正价的数值。11号元素的最外层电子数为1,化合物中显+1价,16号元素的最外层电子数为6,化合物中显-2价,形成化合物的化学式为Na2S;
(2)①从微粒的角度说明图甲反应的实质是氢离子和氢氧根离子生成水分子;图乙所示反应为硫酸铜和锌生成硫酸锌和铜,反应的化学方程式为Zn + Cu SO4== ZnSO4 + Cu;
②复分解反应的实质是溶液中的某些离子结合生成沉淀、气体、水,H2SO4溶液能与BaCl2溶液反应产生白色沉淀,参加反应的离子是Ba2+、SO42-;已知FeCl3溶液能与NaOH溶液反应生成红褐色沉淀,从反应的微观实质可以推测出Fe2(SO4)3溶液可以和氢氧化钡溶液反应同时生成硫酸钡沉淀和氢氧化铁沉淀,该反应的化学方程式Fe 2(SO4)3+3 Ba(OH)2=3 BaSO4↓+2 Fe (OH)3↓。