题目内容
某山区所饮用的水常是河水,由于河水中常含有大量的泥沙、悬浮物和细菌等杂质。可用次氯酸(HClO)杀死细菌,将漂白粉(主要成分是Ca(ClO)2)溶于水可生成氯化钙和次氯酸。下列是某户居民在饮用水之前对河水的处理步骤:
河水 → A(明矾)→ B(沉淀)→ C(过滤)→ D(漂白粉)→ 纯净水
(l)可以除去较大颗粒、悬浮物杂质的步骤是 。(填编号)
(2)能够消毒杀菌的步骤为 。(填编号)
(3)该户居民得到的纯净水是 。(填纯净物,混合物)
(4)如何检验一瓶水是硬水还是软水,请进行实验设计。
| 实验步骤 | 实验现象 | 结论 |
| | | |
(l) C (填编号)(2) D (填编号)(3) 混合物(填纯净物,混合物)
(4)该水是硬水还是软水,请进行实验验证。实验步骤 实验现象 结论 取少量该液体于试管内并滴入几滴肥皂水震荡 出现泡沫 泡沫多的为软水,泡沫少的为硬水
解析试题分析:(1)在净化水时,明矾溶于水后,会形成胶状物吸附水中的泥沙和悬浮物,加速水中的泥沙和悬浮物沉淀,把固体杂质沉至水底,然后过滤才能彻底除去水中的颗粒悬浮物杂质;
(2)漂白粉(主要成分是Ca(ClO)2)溶于水可生成氯化钙和次氯酸,用次氯酸(HClO)杀死细菌病毒,起到消毒杀菌的作用;
(3)经过吸附、沉淀、过滤、消毒杀菌后的水中还含有可溶性杂质,因此是混合物;
(4)检验硬水和软水可用肥皂液,泡沫多的为软水,泡沫少的为硬水
考点:自来水的生产过程与净化方法

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
水对于我们的生产和生活都是非常重要的.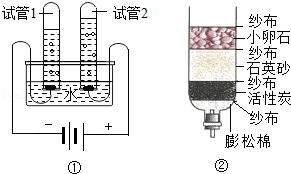
③
| 每100mL含量(μg/100mL) 钙≥400 镁≥50 钾≥35 钠≥80 pH(25℃) 7.3±0.5 |
(1)图①所示电解水的实验中,试管(填“1”或“2”) 中收集的气体是氧气.
(2)小刚要净化收集的雨水,自制了一个简易净水器(如图②所示),其中小卵石、石英沙和膨松棉的作用是 .
(3)某塑料瓶装矿泉水标签如图③所示,饮用该矿泉水,可以为人体提供 2 种营养素.塑料瓶轻便卫生,可回收再利用.其所用材料不属于 .
A.合成材料 B.有机高分子 C.有机物 D.合金
(4)我们应当珍惜每一滴水,下列做法不利于节约用水的是 .
A.洗菜的水用来浇花 B.使用节水龙头
C.用不间断的流水冲洗碗筷 D.洗手擦肥皂时,关上水龙头.
请从下列物质中选择适当的物质填空:(填字母,下同)
| A.肥皂水 | B.氧气 | C.氢气 | D.明矾 |
(3)常用于区分硬水与软水的是 ; (4)常用净水剂是 。