题目内容
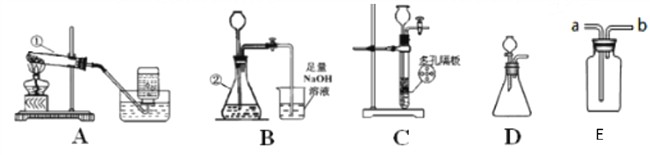
【题目】硝酸铜为蓝色固体,溶于水可得蓝色溶液。某实验小组同学用如图装置加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃。
(提出问题)硝酸铜在加热条件下到底发生了怎样的反应?

(查阅资料)
(1)氧化铜和稀硫酸反应的化学方程式:CuO+H2SO4 ![]() CuSO4+H2O
CuSO4+H2O
(2)含氮化合物中,只有NO2是红棕色、有刺激性气味的气体。
(3)NO2有助燃性,能使带火星的木条复燃
(猜想假设)
Cu(NO3)2受热分解除了生成_____________,还可能生成了CuO和O2。
(进行实验)
实验操作 | 实验现象 | 实验结论 |
(1)将反应后试管中的固体加水充分溶解,过滤,洗涤,向滤渣中加入____________,加热 | 固体全部溶解,得到_____色溶液 | 硝酸铜分解生成了氧化铜。 |
(2)在图A的试管和集气瓶之间连上图B所示的装置,重新进行加热硝酸铜的实验 | 集气瓶中气体为无色,带火星木条复燃 | 硝酸铜分解________(“有”或“无”)氧气生成。 |
步骤(2)是同学们查阅了新的资料后才设计完成的。该资料体现的是有关二氧化氮______的物理性质信息。
(获得结论)根据实验结果,Cu(NO3)2受热分解的化学方程式为________________。
(反思与评价)
已知相同状况下,气体的体积比等于其分子个数比。据此,同学们认为,即使没有资料③,依据实验结论和“加热硝酸铜产生的气体能使带火星的木条复燃”的实验现象,也能推出NO2可能具有助燃性。理由是_____________________。
【答案】 NO2 足量稀硫酸 蓝 有 NO2的沸点(或低温下NO2能否变成液态或固态物质) 2Cu(NO3)2![]() 2CuO+4NO2↑+O2↑ 硝酸铜分解生成的气体中NO2与O2的体积比为4:1,O2所占的体积分数与空气中O2的体积分数基本相同,分解生成气体能使带火星木条复燃而空气不能,说明NO2有助燃性
2CuO+4NO2↑+O2↑ 硝酸铜分解生成的气体中NO2与O2的体积比为4:1,O2所占的体积分数与空气中O2的体积分数基本相同,分解生成气体能使带火星木条复燃而空气不能,说明NO2有助燃性
【解析】根据所学知识和题中信息知,加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃。【提出问题】硝酸铜在加热条件下到底发生了怎样的反应?【猜想假设】Cu(NO3)2受热分解除了生成NO2,还可能生成了CuO和O2,含氮化合物中,只有NO2是红棕色、有刺激性气味的气体,)NO2有助燃性,能使带火星的木条复燃。【进行实验】
实验操作 | 实验现象 | 实验结论 |
(1)将反应后试管中的固体加水充分溶解,过滤,洗涤,向滤渣中加入足量稀硫酸,加热 | 固体全部溶解,得到蓝色溶液 | 硝酸铜分解生成了氧化铜,氧化铜呈黑色,氧化铜与硫酸反应生成硫酸铜蓝色溶液。 |
(2)在图A的试管和集气瓶之间连上图B所示的装置,重新进行加热硝酸铜的实验 | 集气瓶中气体为无色,带火星木条复燃 | 硝酸铜分解有氧气生成,氧气可以使带火星木条复燃。 |
步骤(2)是同学们查阅了新的资料后才设计完成的。该资料体现的是有关二氧化氮的沸点(或低温下NO2能否变成液态或固态物质)的物理性质信息。【获得结论】根据实验结果,Cu(NO3)2受热分解的化学方程式为2Cu(NO3)2![]() 2CuO+4NO2↑+O2↑。【反思与评价】相同状况下,气体的体积比等于其分子个数比。依据实验结论和“加热硝酸铜产生的气体能使带火星的木条复燃”的实验现象,也能推出NO2可能具有助燃性。理由是硝酸铜分解生成的气体中NO2与O2的体积比为4:1,O2所占的体积分数与空气中O2的体积分数基本相同,分解生成气体能使带火星木条复燃而空气不能,说明NO2有助燃性。
2CuO+4NO2↑+O2↑。【反思与评价】相同状况下,气体的体积比等于其分子个数比。依据实验结论和“加热硝酸铜产生的气体能使带火星的木条复燃”的实验现象,也能推出NO2可能具有助燃性。理由是硝酸铜分解生成的气体中NO2与O2的体积比为4:1,O2所占的体积分数与空气中O2的体积分数基本相同,分解生成气体能使带火星木条复燃而空气不能,说明NO2有助燃性。
点睛∶这是一道实验探究题,Cu(NO3)2受热分解除了生成NO2,还可能生成了CuO和O2。含氮化合物中,只有NO2是红棕色、有刺激性气味的气体。)NO2有助燃性,能使带火星的木条复燃。