题目内容
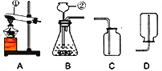
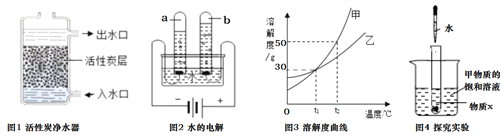
【题目】Ⅰ.下列各图是进行O2、CO2的实验室制取和有关性质的实验装置.
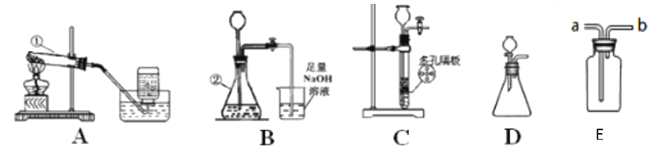
(1)标号仪器的名称:①______________②______________。
(2)用氯酸钾固体制取O2,应选用上图中的_____装置(填字母);反应的化学方程式为______。
(3)能控制反应速率的气体发生装置为____________,写出此装置制取氧气的化学方程式___________;若用E装置排水取气法收集一瓶氧气,气体应从_____端进入(填a或b)。
(4)用稀盐酸和大理石在B装置中反应制取CO2化学方程式为___________________。检验二氧化碳有关性质,观察到烧杯中导管口有气泡冒出,但无其它明显现象.若证明CO2与NaOH溶液发生了化学反应,以下方案不合理的是______________(填序号).
A.取少量烧杯中液体滴加无色酚酞 B.取少量烧杯中液体滴加足量稀盐酸
C.取少量烧杯中液体滴加氯化钙溶液 D.取少量烧杯中液体滴加氢氧化钙溶液,若用上述实验方案测出CO2与NaOH溶液发生了化学反应,反应的化学方程式为______
(5)用C装置代替B中的气体发生装置制备CO2,优点是___________________________;
【答案】 试管 锥形瓶 A 2KClO3 ![]() 2KCl+3O2↑ D 2H2O2
2KCl+3O2↑ D 2H2O2 ![]() 2H2O+O2↑ b CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ A 2NaOH+CO2==Na2CO3+H2O 控制反应的发生和停止
2H2O+O2↑ b CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ A 2NaOH+CO2==Na2CO3+H2O 控制反应的发生和停止
【解析】(1)图中①是试管,②是锥形瓶;
(2)用氯化钾固体制取O2,是固体的加热反应,氧气不易溶于水,所以可用装置A进行,反应方程式是:2KClO3 ![]() 2KCl+3O2↑;
2KCl+3O2↑;
(3)装置D中可以控制分液漏斗的活塞来控制液体的加入量,从而控制反应速率;适用于过氧化氢制氧气,化学方程式为:2H2O2 ![]() 2H2O+O2↑;由于氧气的密度小于水,所以氧气应从b管进入将水从a管排除;
2H2O+O2↑;由于氧气的密度小于水,所以氧气应从b管进入将水从a管排除;
(4)大理石的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl =CaCl2 +H2O+CO2↑;A、二氧化碳与氢氧化钠反应生成碳酸钠溶液显碱性,反应发生变红,不反应也变红,错误;B、碳酸钠和稀盐酸反应有二氧化碳气体生成,可以证明CO2与NaOH溶液发生了化学反应,正确;C、碳酸钠和氯化钙反应生成碳酸钙沉淀,可以证明CO2与NaOH溶液发生了化学反应,正确;D、碳酸钠和石灰水反应生成碳酸钙沉淀,可以证明CO2与NaOH溶液发生了化学反应,正确。二氧化碳与氢氧化钠反应生成碳酸钠和水,化学方程式为:2NaOH+CO2=Na2CO3+H2O;
(5)通过C装置中的多孔隔板和阀门可以随时控制反应的发生和停止。

 金钥匙试卷系列答案
金钥匙试卷系列答案【题目】硝酸铜为蓝色固体,溶于水可得蓝色溶液。某实验小组同学用如图装置加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃。
(提出问题)硝酸铜在加热条件下到底发生了怎样的反应?
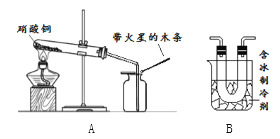
(查阅资料)
(1)氧化铜和稀硫酸反应的化学方程式:CuO+H2SO4 ![]() CuSO4+H2O
CuSO4+H2O
(2)含氮化合物中,只有NO2是红棕色、有刺激性气味的气体。
(3)NO2有助燃性,能使带火星的木条复燃
(猜想假设)
Cu(NO3)2受热分解除了生成_____________,还可能生成了CuO和O2。
(进行实验)
实验操作 | 实验现象 | 实验结论 |
(1)将反应后试管中的固体加水充分溶解,过滤,洗涤,向滤渣中加入____________,加热 | 固体全部溶解,得到_____色溶液 | 硝酸铜分解生成了氧化铜。 |
(2)在图A的试管和集气瓶之间连上图B所示的装置,重新进行加热硝酸铜的实验 | 集气瓶中气体为无色,带火星木条复燃 | 硝酸铜分解________(“有”或“无”)氧气生成。 |
步骤(2)是同学们查阅了新的资料后才设计完成的。该资料体现的是有关二氧化氮______的物理性质信息。
(获得结论)根据实验结果,Cu(NO3)2受热分解的化学方程式为________________。
(反思与评价)
已知相同状况下,气体的体积比等于其分子个数比。据此,同学们认为,即使没有资料③,依据实验结论和“加热硝酸铜产生的气体能使带火星的木条复燃”的实验现象,也能推出NO2可能具有助燃性。理由是_____________________。