题目内容
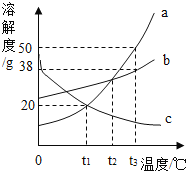
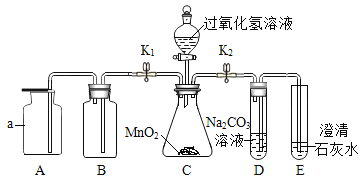
【题目】有一包白色粉末,可能含有K2SO4、Na2CO3、BaCl2、CuSO4中的一种或几种。取样溶于足量的水,有白色沉淀产生,过滤,滤液呈无色;向沉淀中滴加稀盐酸,产生沉淀的质量与加入盐酸体积的关系如图所示。由此推断白色粉末的成分是( )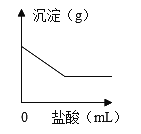
A. 可能有 BaCl2 B. 可能有Na2SO4
C. 肯定只有Na2CO3 D. 肯定有K2SO4、Na2CO3、BaCl2,没有CuSO4
【答案】D
【解析】图象中沉淀的量先是下降然后不变,说明生成的沉淀中既有能与盐酸反应的碳酸钡(碳酸钠和氯化钡反应得到)又有不能溶于盐酸的硫酸钡(硫酸钾和氯化钡反应生成的),由于过滤,滤液呈无色,所以固体中不可能含有硫酸铜(硫酸铜的溶液呈蓝色)所以白色固体中一定含有硫酸钾、碳酸钠和氯化钡,一定不含硫酸铜。故选D。

 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
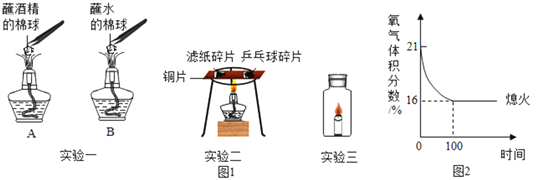
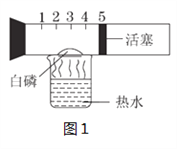
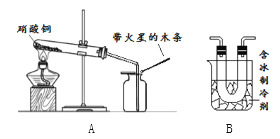
单元期中期末卷系列答案【题目】硝酸铜为蓝色固体,溶于水可得蓝色溶液。某实验小组同学用如图装置加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃。
(提出问题)硝酸铜在加热条件下到底发生了怎样的反应?
(查阅资料)
(1)氧化铜和稀硫酸反应的化学方程式:CuO+H2SO4 ![]() CuSO4+H2O
CuSO4+H2O
(2)含氮化合物中,只有NO2是红棕色、有刺激性气味的气体。
(3)NO2有助燃性,能使带火星的木条复燃
(猜想假设)
Cu(NO3)2受热分解除了生成_____________,还可能生成了CuO和O2。
(进行实验)
实验操作 | 实验现象 | 实验结论 |
(1)将反应后试管中的固体加水充分溶解,过滤,洗涤,向滤渣中加入____________,加热 | 固体全部溶解,得到_____色溶液 | 硝酸铜分解生成了氧化铜。 |
(2)在图A的试管和集气瓶之间连上图B所示的装置,重新进行加热硝酸铜的实验 | 集气瓶中气体为无色,带火星木条复燃 | 硝酸铜分解________(“有”或“无”)氧气生成。 |
步骤(2)是同学们查阅了新的资料后才设计完成的。该资料体现的是有关二氧化氮______的物理性质信息。
(获得结论)根据实验结果,Cu(NO3)2受热分解的化学方程式为________________。
(反思与评价)
已知相同状况下,气体的体积比等于其分子个数比。据此,同学们认为,即使没有资料③,依据实验结论和“加热硝酸铜产生的气体能使带火星的木条复燃”的实验现象,也能推出NO2可能具有助燃性。理由是_____________________。
【题目】阅读下面科普短文。
(资料1)融雪剂按组成分为有机融雪剂和无机融雪剂。
有机融雪剂的主要成分为醋酸钾,一般用于机场等重要场所。
无机融雪剂以氯化钠、氯化钙等为主要成分,其融雪原理与相同条件下,不同浓度的食盐水的凝固点有关(见下表)。
溶剂质量(g) | 100 | 100 | 100 | 100 | 100 |
溶质质量(g) | 0 | 3.6 | 7.5 | 11.1 | 29.9 |
凝固点(℃) | 0 | -2.3 | -4.2 | -6.3 | -21 |
(资料2)钛(Ti)是一种银白色的金属。它具有良好的耐高温、耐低温、抗酸碱以及高强度、低密度的特点,广泛用于航空工业;它无毒且具有优良的生物相容性,是非常理想的医用金属材料,可用来制造人造骨等。金属钛不仅能在空气中燃烧,也能在二氧化碳或氮气中燃烧。在稀有气体和高温条件下,用四氯化钛和镁发生置换反应可制备金属钛。
依据资料,回答下列问题:
(1)若飞机场使用融雪剂,应选择融雪剂的类别是___________。
(2)从无机融雪剂的融雪原理得出:100g溶剂中,溶质质量和凝固点的关系是_______________。
(3)钛金属广泛应用于航空工业的原因是____________________(答出2条即可)。
(4)金属钛着火时___________(填“能”或“不能”)用二氧化碳灭火。
(5)四氯化钛制备金属钛的化学方程式是__________________________________。