题目内容
【题目】阅读下面科普短文。
黄石被称为世界青铜文化的发祥地。青铜古称“吉金”,多为金黄色,主要是铜、锡、铅的合金。因其铜锈呈青绿色, 故名青铜。运用现代仪器分析青铜器及其锈蚀成分可以帮助我们对青铜器文物进行研究和保护。
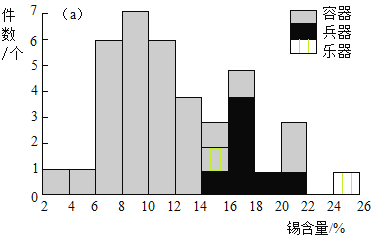
研究人员利用X射线能谱仪对我国西周晚期某墓地出土的青铜容器、兵器、乐器的成分进行了分析,其中锡含量的分布频次如图。
研究人员利用X射线衍射分析技术对“镇国之宝”后母戊鼎西南足部位的锈蚀样品进行分析,结果如下:
锈蚀成分 样品编号 | Cu2Cl(OH)3 | Cu2O | Cu2CO3(OH)2 | SnO2 | 其他 |
1 | 98% | 2% | 0 | 0 | 0 |
2 | 5% | 95% | 0 | 0 | 0 |
3 | 29% | 34% | 12% | 0 | 25% |
4 | 61% | 0 | 4% | 9% | 26% |
上述成分中,碱式氯化铜[Cu2Cl(OH)3]对青铜文物的危害极大,器物一旦沾染上这种物质,在环境湿度适宜的条件下,就会像患上瘟疫一样传染和蔓延,将会造成溃烂、穿孔,直至彻底瓦解。
依据文章内容回答下列问题。
(1)青铜器属于_________。
A 金属材料 B 合成材料
(2)由锡含量的分布频次图推断,某件青铜兵器的锡含量可能是_____
A 4% B 18%
(3)后母戊鼎西南足上的锈蚀成分中,Cu2O属于__________。
A 氧化物 B 盐
(4)碱式氯化铜[Cu2Cl(OH)3]的生成与环境中的氧气、水和_________密切相关。
A 氯化物 B 二氧化碳
(5)请你对保存珍贵的青铜器提出一条合理化建议____________。
【答案】A B A A 为了防止青铜器的锈蚀,避免将其放置在潮湿,并含有氯化物和氧气的环境中
【解析】
(1)由题干可知,青铜主要是铜、锡、铅的合金,合金属于金属材料,故填写:A;
(2)由图可知,青铜兵器的锡含量在14%-22%范围内,因此,B选项的18%在此范围内,故填写:B;
(3)Cu2O是由氧元素和铜元素组成,根据氧化物的定义可知,Cu2O属于氧化物,故填写:A;
(4)根据质量守恒定律的实质:化学反应前后,元素种类不变原则可知,Cu2Cl(OH)3中含有铜元素、氯元素、氧元素、氢元素,因此,它的生成与环境中的氧气、水和氯化物密切相关,故填写:A;
(5)碱式氯化铜[Cu2Cl(OH)3]对青铜文物的危害极大,由(4)可知,碱式氯化铜的生成与环境中的氧气、水和氯化物密切相关,因此,为了防止青铜器的锈蚀,避免将其放置在潮湿,并含有氯化物和氧气的环境中,故填写:为了防止青铜器的锈蚀,避免将其放置在潮湿,并含有氯化物和氧气的环境中。

 阅读快车系列答案
阅读快车系列答案【题目】在过氧化氢溶液的分解反应中,某化学兴趣小组发现:除了二氧化锰,硫酸铜溶液也能对H2O2的分解起催化作用。对此,他们进行了有关探究。
(提出问题)CuSO4溶液是混合物,是其中哪一种成分起到了催化作用呢?
(查阅资料)①稀硫酸中主要含有H2O、H+、SO42三种微粒。
②CuSO4溶液中主要含有H2O、Cu2+、SO42三种微粒。
(作出猜想)根据以上信息,同学们作出了如下三个猜想:
Ⅰ:SO42催化分解H2O2 Ⅱ:Cu2+催化分解H2O2 Ⅲ:H2O催化分解H2O2
(1)其中,明显不合理的是_______(填序号),理由是_______。
(实验验证)
(2)为了验证自己的猜想,同学们设计了如下两个实验(所取H2O2溶液的浓度相同):
操作 | 现象 | 结论 |
取5 mL H2O2溶液于试管中,滴入少量的稀硫酸,伸入带火星的木条 | _______ | SO42对H2O2的分解不起催化作用 |
_______ | 产生大量气泡,带火星的木条复燃 | _______ |
(实验拓展)
实验一:用图甲装置探究影响H2O2分解速率的因素,得到图乙、图丙所示曲线(在等温条件下,产生氧气体积与装置内压强成正比,反应放热忽略不计)。
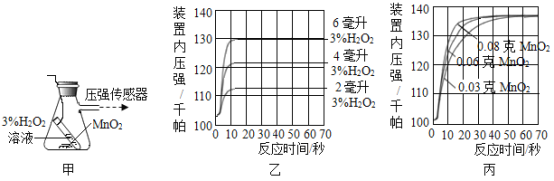
(3)写出图甲中反应的化学方程式_______。
(4)图乙是“0.1 g MnO2与不同体积的3% H2O2溶液混合”的实验结果,从图中可以看出_______。
(5)图丙是用“8 mL浓度为3%的H2O2溶液与不同质量的MnO2混合”时,所得到的曲线,通过该曲线可以得到的结论是_______。
实验二:用图丁装置探究氧气的浓度对燃烧的影响。点燃蜡烛后立即塞紧橡皮塞,待蜡烛熄灭后,将滴管中的水全部滴入瓶中,铝盒中的白磷燃烧。
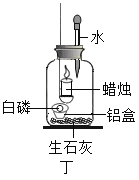
(6)白磷燃烧的主要现象是_______。
(7)由“蜡烛熄灭,白磷燃烧”可得出的结论是_______。
(8)滴入水后白磷燃烧的原因是_______。
【题目】某化学活动小组在一次实验中进行如下所示实验:
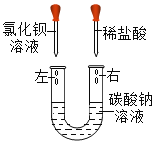
此时观察到U型管右侧产生的现象是___________________________,实验后,小组同学充分振荡U型管,发现管内仍有白色固体残留,将混合物过滤后,同学们对滤液成分产生了浓厚的兴趣,于是进行了进一步的探究活动。
(提出问题):滤液中可能含有哪些物质?
(猜想与假设):猜想一:溶质为NaCl
猜想二:溶质为NaCl和BaCl2
猜想三:溶质为______
(实验探究):小红为验证滤液的成分,取滤液于试管中,向其中滴加少量的硫酸钠溶液,观察到无明显现象。由此得出结论:猜想一成立。小刚认为小红的结论不严密,因为____________________________。
为验证三的猜想请填写下表:
实验过程 | 实验现象 | 实验结论 |
取少量滤液滴加_____ | 溶液变红 | 猜想三正确 |
(归纳与总结):通过上述实验我们能够总结出:在确定化学反应前后所得溶液中溶质成分时除了考虑生成物外,还要考虑__________________________。
【题目】一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
纯净物 | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
反应前质量/g | 2.3 | 4 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 2.2 | 2.7 | 待测 |
A.反应后X的质量为1.5g B.X中一定含有碳元素和氧元素
C.X中一定含有碳元素和氢元素 D.X中两种元素的质量比是1:1