题目内容
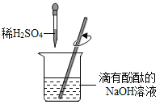
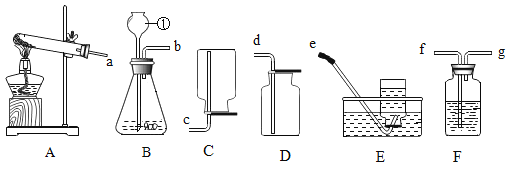
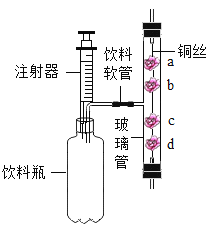
【题目】实验室现有稀硫酸、浓硫酸、锌粒、硫酸铜溶液、氧化铜、水等药品。某同学选用这些药品设计如图装置制备单质铜。

(1)写出装置A中发生反应的化学方程式__________。
(2)装置B中的试剂是______,其作用是__________。
(3)在点燃装置C中酒精灯之前的操作是__________。
(4)该同学用32.5g锌充分反应,能否制得32g铜?____(填“能”或“否”)。
【答案】![]() 浓硫酸 干燥氢气 先通入一会儿氢气,排净装置内的空气 否
浓硫酸 干燥氢气 先通入一会儿氢气,排净装置内的空气 否
【解析】
(1)装置A中是锌和稀硫酸反应制取氢气,反应的化学方程式为![]() 。
。
(2)装置B中的试剂是浓硫酸,浓硫酸有强吸水性,用于干燥氢气。
(3)氢气具有可燃性,所以在点燃装置C中的酒精灯前一定要先通入氢气排净装置内的空气,以防发生爆炸。
(4)设32.5g锌与硫酸反应生成氢气的质量为x,则:
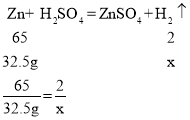
x=1g
设1g氢气与氧化铜充分反应生成铜的质量为y
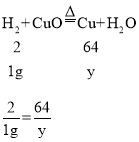
y=32g
根据化学方程式,理论上用32.5g锌充分反应,刚好制得32g铜,但该装置内有空气,在加热前要先通入氢气,把装置内的空气排出,要消耗一定量的氢气,所以制得的铜的质量必然小于32g。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目