题目内容
【题目】今年全省统一的化学实验操作考试中,有一题目是鉴别澄清石灰水和氢氧化钠溶液。实验考试中小苗等几位同学碰到了如下问题,请你参与探究:
(提出问题)如何鉴别这两种无色溶液?
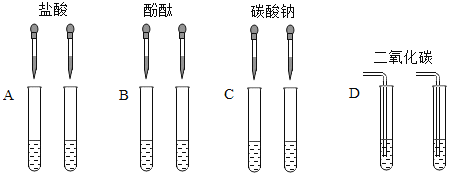
(实验方案)小苗等几位同学进行了下图所示的实验。请你回答下列问题:
(1)C组实验中反应的化学方程式为____;
(2)其中不能达到实验目的的是(填字母)____;
(3)实验结束后,小苗同学将D组的两支试管中的废液倒入同一个干净的烧杯中,并将废液进行过滤,同学们对滤液成分进行了探究。
(提出问题)滤液中除水外还含有哪些物质?
(查阅资料)氯化钙溶液呈中性;
(猜想假设)a:只含有氢氧化钠;b:只含有碳酸钠;c:含有氢氧化钠和氢氧化钙;
你认为还可能是(写一种猜想)_____
(实验设计)设计一个简单的实验证明你的猜想正确。
实验步骤 | 实验现象 | 实验结论 |
取滤液于试管中,_______ | ______________________ | 猜想正确 |
(反思拓展)
下列实验方法可以区分氢氧化钠和氢氧化钙两种固体的是____(填字母)。
A 放置在空气中 B 观察颜色 C 加水溶解 D 利用溶解性
【答案】Na2CO3+Ca(OH)2═CaCO3↓+2NaOH AB 氢氧化钠和碳酸钠 加入足量氯化钙溶液,静置,滴加酚酞试液 产生白色沉淀,溶液变红色 ACD
【解析】
(1)C组实验中碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(2)A中反应过程中都无明显现象,因此滴加盐酸不能区分氢氧化钠溶液和氢氧化钙溶液;
B过程中溶液都变红色,滴加酚酞试液不能区分氢氧化钠溶液和氢氧化钙溶液;
C澄清石灰水与碳酸钠溶液反应会产生白色沉淀,氢氧化钠无明显现象,可以区分;
D二氧化碳通入澄清石灰水中会产生白色沉淀,通入氢氧化钠中无明显现象,可以区分;
(3)[猜想假设]a:氢氧化钠和二氧化碳恰好完全反应,氢氧化钙和二氧化碳反应后氢氧化钙过量,过量的氢氧化钙和碳酸钠前后完全反应时只含有氢氧化钠;
b:氢氧化钠和二氧化碳恰好完全反应,氢氧化钙和二氧化碳恰好完全反应时只含有碳酸钠;
c:氢氧化钠和二氧化碳恰好完全反应,氢氧化钙和二氧化碳反应后氢氧化钙过量,碳酸钠和氢氧化钙反应后氢氧化钙过量时含有氢氧化钠和氢氧化钙;
氢氧化钠和二氧化碳恰好完全反应或氢氧化钠过量,氢氧化钙和二氧化碳反应后氢氧化钙过量或恰好完全反应,碳酸钠和氢氧化钙反应后碳酸钠过量或碳酸钠不能反应时是氢氧化钠和碳酸钠;
[实验设计]取滤液于试管中,加入足量氯化钙溶液,静置,滴加酚酞试液,产生白色沉淀,是因为碳酸钠和氯化钙反应生成了白色沉淀碳酸钙,溶液变红色,是因为溶液中含有氢氧化钠;
[反思拓展]A、放置在空气中时,由于氢氧化钠能够吸收空气中的水蒸气,一段时间后会潮解,而氢氧化钙不能发生潮解,能够区分氢氧化钠和氢氧化钙;
B、氢氧化钠和氢氧化钙都是白色固体,通过观察颜色不能区分氢氧化钠和氢氧化钙;
C、加水溶解时,氢氧化钠溶于水放热,氢氧化钙溶于水无明显现象,能够区分氢氧化钠和氢氧化钙;
D、氢氧化钠易溶于水,氢氧化钙微溶于水,利用溶解性能够区分氢氧化钠和氢氧化钙。

 优等生题库系列答案
优等生题库系列答案