题目内容
【题目】葡萄糖是生命体所需能量的主要来源。
(提出问题)葡萄糖的燃烧产物是CO2和H2O,由此能否证明:葡萄糖只由碳元素和氢元素组成的有机物?
(实验设计)为了确定葡萄糖的元素组成,某小组设计了如图的实验流程(其中浓硫酸、无水CaCl2均为常用干燥剂,部分固定装置省略)。
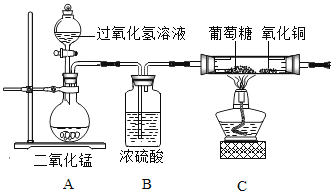
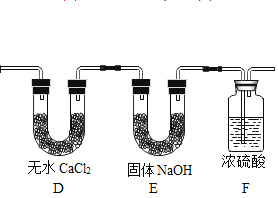
(1)装置B中浓硫酸的作用是__________________。
(2)装置C处氧化铜的作用是_________________。
(方案评价)
(1)用充有空气的储气球代替装置A,是否更有利于实验的进行?________(填“是”或“否”)原因是______________。
(2)装置D和E______________(填“能”或“不能”)对调,原因是_____________。
(数据处理)下表3是同学们填写的实验报告,请你帮助完成。
实验事实 | 数据分析及结论 |
1.8g葡萄糖完全燃烧,得到2.64g CO2和1.08g H2O | 数据___________ 结论:葡萄糖含有C、H、O三种元素 |
(讨论交流)为了尽量减少误差:
(1)该实验在进行过程中应注意的问题是________________(写1条)。
(2)从定量实验的角度看,该实验是否可进一步改进?请简要写出一个改进意见:___________。
【答案】干燥A装置中产生的氧气 将葡萄糖不完全燃烧产生的少量一氧化碳氧化变为二氧化碳,保证葡萄糖中的碳全部转化为二氧化碳气体 否 空气中含有少量二氧化碳,会干扰实验结果的测定 不能 固体氢氧化钠可同时吸收水蒸气和二氧化碳,不能分别确定燃烧产物水和二氧化碳的质量 2.46g二氧化碳中含有碳元素质量=2.64g×![]() 0.72g,
0.72g,
1.08g水中含有氢元素质量=1.08g×![]() ,
,
碳元素与氢元素质量之和=0.72g+0.12g=0.84g,小于1.8g葡萄糖质量; 实验前应该先通入氧气,在进行加热,防止一开始的葡萄糖不充分燃烧 将F装置的浓硫酸洗气瓶换成装有氢氧化钠的干燥管,可以同时吸收空气中水和二氧化碳,减少实验误差
【解析】
(1)装置B中浓硫酸具有吸水性,作用是:干燥A装置中产生的氧气;
(2)装置C处氧化铜的作用是:将葡萄糖不完全燃烧产生的少量一氧化碳氧化变为二氧化碳,保证葡萄糖中的碳全部转化为二氧化碳气体;
方案评价
(1)用充有空气的储气球代替装置A,不更有利于实验的进行,原因是:空气中含有少量二氧化碳,会干扰实验结果的测定;
(2)装置D和E不能对调,原因是:固体氢氧化钠可同时吸收水蒸气和二氧化碳,不能分别确定燃烧产物水和二氧化碳的质量;
【数据处理】
下表3是同学们填写的实验报告,请你帮助完成。
2.46g二氧化碳中含有碳元素质量=2.64g×![]() 0.72g,
0.72g,
1.08g水中含有氢元素质量=1.08g×![]() ,
,
碳元素与氢元素质量之和=0.72g+0.12g=0.84g,小于1.8g葡萄糖质量;
则葡萄糖含有C、H、O三种元素;
讨论交流
(1)该实验在进行过程中应注意的问题是:实验前应该先通入氧气,在进行加热,防止一开始的葡萄糖不充分燃烧;
(2)从定量实验的角度看,该实验是需要改进:将F装置的浓硫酸洗气瓶换成装有氢氧化钠的干燥管,可以同时吸收空气中水和二氧化碳,减少实验误差。

【题目】某校化学兴趣小组利用下列仪器在实验室进行制取O2的相关实验探究,请回答下列问题.
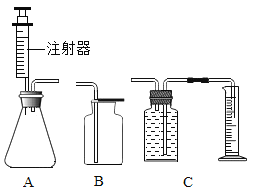
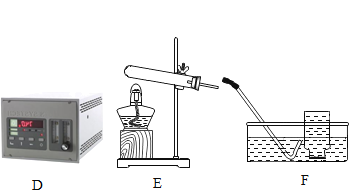
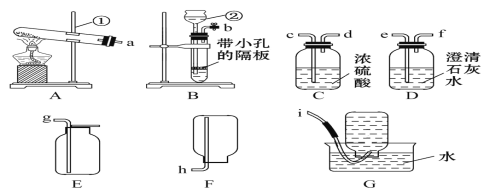
(1)甲小组用MnO2、KClO3两种药品制取干燥的O2,需选用的仪器组合是________,反应结束后回收MnO2固体,操作依次是冷却至室温、________、过滤、________、烘干.
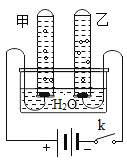
(2)乙小组探究Fe2O3能否作为H2O2分解的催化剂.实验时间为30s(H2O2过量),其他可能影响实验的因素均保持不变,相关数据如下:
实验序号 | 10%的H2O2溶液(mL) | 溶液中加入物质(g) | 收集到气体的 体积(mL) |
1 | 100 | 无 | a |
2 | 100 | Fe2O30.5g | b |
3 | 100 | MnO20.5g | c |
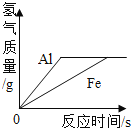
通过比较和______(填“a”“b”“c”)的大小,可证明Fe2O3在实验中起催化作用,写出该反应的化学方程式________.其次需补做实验,验证反应前后Fe2O3的化学性质不变和验证________.
(3)丙小组探究MnO2的用量对H2O2分解速率的影响.每次均用30mL10%的H2O2溶液,使用不同质量的MnO2作催化剂,测定每次收集到500mL O2所用的时间.结果如图(其他实验条件相同):
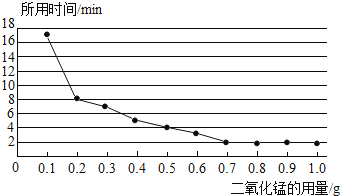
由图可知,MnO2的用量对H2O2分解速率影响的规律是①________; ②MnO2的用量超出一定范围后,其用量再增大,反应速率不再继续加快.