题目内容
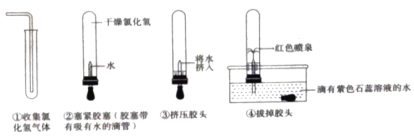
【题目】化学兴趣小组为验证质量守恒定律,做镁条在空气中燃烧的实验(如图1)。同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体。

(1)镁条燃烧的化学方程式是_____;
(2)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量。小马认为这个反应不遵循质量守恒定律。你_____(“同意”或“不同意”)他的观点。你认为出现这样实验结果的原因可能是_____。
(3)小红按如图2装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体。
(提出问题)黄色固体是什么?
(查阅资料)①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)
固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
(做出猜想)黄色固体是Mg3N2
(实验探究)请设计实验,验证猜想
实验操作 | 实验现象 | 实验结论 |
将收集到的黄色固体放入试管中,加入适量的_____,在试管口放置湿润红色石蕊试纸。 | ①_____; ②_____。 | 黄色固体是Mg3N2 |
(反思与交流)空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是_____。
【答案】2Mg+O2![]() 2MgO 不同意 反应生成的氧化镁部分扩散到空气中 水 产生气泡 湿润红色石蕊试纸变蓝色 相同条件下,镁更容易和氧气反应
2MgO 不同意 反应生成的氧化镁部分扩散到空气中 水 产生气泡 湿润红色石蕊试纸变蓝色 相同条件下,镁更容易和氧气反应
【解析】
(1)镁条燃烧水槽氧化镁,反应的化学方程式为:2Mg+O2![]() 2MgO。故答案为:2Mg+O2
2MgO。故答案为:2Mg+O2![]() 2MgO。
2MgO。
(2)不同意他的观点,出现这样实验结果的原因可能是反应生成的氧化镁部分扩散到空气中。故答案为:不同意;反应生成的氧化镁部分扩散到空气中。
(3)【实验探究】实验过程如下所示:
实验操作 | 实验现象 | 实验结论 |
将收集到的黄色固体放 入试管中,加入适量的水,在试管口放 置湿润红色石蕊试纸。 | ①产生气泡; ②湿润红色石蕊试纸变蓝色。 | 黄色固体是Mg3N2 |
【反思与交流】空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是相同条件下,镁更容易和氧气反应。故答案为:相同条件下,镁更容易和氧气反应。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案【题目】兴趣小组的同学学习了金属的性质后,在实验室找到的一种银白色金属R做如下探究:
(1)将金属R投入稀盐酸中,金属表面有气泡冒出.则该金属R在金属活动性顺序表中排在氢的 (选填“前面”或“后面”)。
(2)为了比较金属R与铁的活动性强弱,兴趣小组设计下列方案进行实验,请完成下表:
你的一种猜想 | 验证方法 | 现象 | 结论 |
金属R的活动性比铁 | 将金属R投入 溶液中 | 金属R表面有黑色的物质析出 | 猜想 (选填“正确”或“错误”) |
(3)请根据上述的信息,标出金属Fe、R、Cu在下列金属活动性顺序表中的相应位置。