��Ŀ����
����Ŀ���£�N2H4���ǵ�Ԫ�غ���Ԫ���γɵ�һ�ֻ����������ˮ����ҵ���������ط������£�ͬʱ�õ�����Ʒ̼���ƾ��壬�乤���������£�
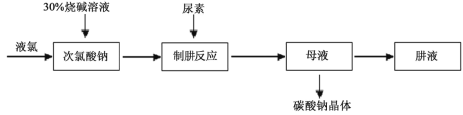
��1��ʵ������У����µĻ�ѧ��Ӧ����ʽΪ��CO(NH2)2 + NaClO + 2NaOH�TN2H4 + Na2CO3 + H2O + _____���ѧʽ����
��2��ʵ�������� 30%�ռ���Һ������IJ���������_____������ţ���
A ©�� B �ձ� C ��ƿ D ��Ͳ E ������
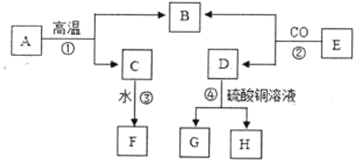
��3����ʵ�����У��Ӳ����͵�̼����ĸҺ����Һ�з����̼���ƾ��壬���Բ��õIJ��� ����Ϊ_____������ţ����ˣ�����ʱ����Һ�������ֽ��Ե���ᵼ�µõ���̼���ƾ�������_______������ƫ��������ƫ��������
A ���� B ���� C ���� D ���� E ��ȴ�ᾧ
���𰸡�![]() B D E E D ƫ��
B D E E D ƫ��
��������
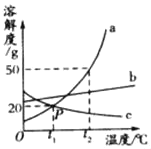
������ˮ��Ӧ�����ᣬ���������кͷ�Ӧ��̼���Ƶ��ܽ�����¶ȱ仯�Ƚϴ���Һ�нᾧ�����ķ�������ȴ�ȱ�����Һ�ķ�����
��1�����������غ㶨�ɣ�ʵ������У����µĻ�ѧ��Ӧ����ʽΪ��![]() ��
��
��2��ʵ�������� 30%�ռ���Һ���ܽ���Ҫ�ձ���ת��Һ����Ҫ����������ȡҺ����Ҫ��Ͳ������IJ���������B��D��E��
��3��̼���Ƶ��ܽ�����¶ȱ仯�Ƚϴ���Һ�нᾧ�����ķ�������ȴ�ȱ�����Һ�ķ�������ʵ�����У��Ӳ����͵�̼����ĸҺ����Һ�з����̼���ƾ��壬���Բ��õIJ�������ΪE D������ʱ����Һ�������ֽ��Ե��������Һ���࣬�õ���̼���ƾ����������٣��ʵõ���̼���ƾ�������ƫ�͡�

 ��Уͨ��֤��Ч��ҵϵ�д�
��Уͨ��֤��Ч��ҵϵ�д�