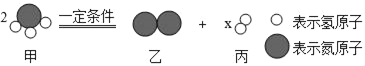��Ŀ����
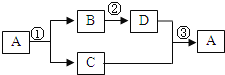
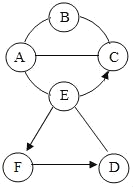
����Ŀ��ͼ��A��B��C��D��E��F�ֱ��ʾ�������ʣ�B��C��D��F�ֱ������ᡢ��Ρ���������������е�һ�֣�A��Ŀǰ�����������ߵĽ�����B�ǿ��������Σ�D��E�����ķ�Ӧ�����кͷ�Ӧ(ͼ��������������������ʾ��������֮���ܷ�����ѧ��Ӧ��������������![]() ����ʾһ�����ʿ�ת��Ϊ��һ�����ʣ����ַ�Ӧ��������P��Ӧ��������ȥ��ͼ�и����ַ�Ӧ������Һ�н���)������˵������ȷ����( )
����ʾһ�����ʿ�ת��Ϊ��һ�����ʣ����ַ�Ӧ��������P��Ӧ��������ȥ��ͼ�и����ַ�Ӧ������Һ�н���)������˵������ȷ����( )
A. D������Ca(OH)2
B. Eת��ΪF������Ӧ�Ļ�ѧ����ʽ������2NaOH+H2SO4�TNa2SO4+2H2O
C. ������Ӧ���漰�����ֻ�����Ӧ����
D. B��C������Ӧ��ʵ���������а�ɫ��������
���𰸡�C
��������
B��C��D��F�ֱ������ᡢ��Ρ���������������һ�֣�A��Ŀǰ�����������ߵĽ���������A������B�ǿ��������Σ�����B����������D��E�����ķ�Ӧ�����кͷ�Ӧ��A����E��Ӧ������E���������ᣬE��ת����F��F��ת����D��D�Ǽ����D���������ƣ�F��ˮ������ת���ɵ�C����������������Ӧ������C���Ȼ�ͭ��������֤���Ƶ���ȷ��
A��D�Ǽ����D���������ƣ���A��ȷ��
B��E���ᣬ���������ᣬF��ˮ��Eת��ΪF������Ӧ�Ļ�ѧ����ʽ�����ǣ�2NaOH+H2SO4�TNa2SO4+2H2O����B��ȷ��
C��������Ӧ��û���漰�û���Ӧ����C����
D��B����������C���Ȼ�ͭ��B��C��Ӧ���ɰ�ɫ���Ȼ�����������D��ȷ��

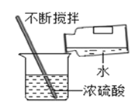
����Ŀ��Ϊ�ⶨij��ʯ��ʯ��̼��Ƶ�����������ij��ȤС�齫һ��������ʯ��ʯ��Ʒ�����ֳ����ȷݣ���������ʵ�飺
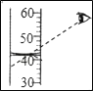
(1)һ�ݷ����ձ��У����ձ�������ijһŨ�ȵ����ᣬ��Ӧ���̲��ʣ�������������������������ϵ��ͼ��ʾ(ʯ��ʯ�е����ʲ������ᷴӦ��Ҳ������ˮ)����ش��������⣺
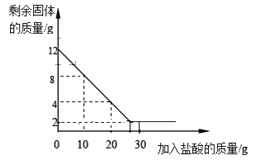
��ʯ��ʯ��Ʒ��̼��Ƶ���������________��
��ͨ�����������������������������Ϊ__________��
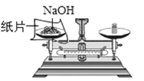
(2)��һ�ݽ�������ͼ��ʾ��ʵ�飺�Ѳ�����CO2�������������ռ���Һ���գ�ͬʱ����Bƿ�ռ���Һ���ӵ�������������±���ʾ��
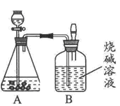
ʱ��/�� | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
B���ӵ����� | 0 | 2 | 3 | 4 | 4.6 | X | 4.6 |
�����ϱ��У���5����ʱ��x=______________��
�ڸ�ʵ������Ʒ��̼��Ƶ���������_________(����ڡ�С�ڻ����)��һʵ�飬��ԭ�������______________________________��