题目内容
【题目】某同学在家中找到一种白色粉末,到学校实验室进行实验,实验过程与现象如下:
![]()
对此粉末成分判断正确的是( )
A. 该粉末一定是碳酸钙 B. 该粉末可能是碳酸钠或碳酸氢钠
C. 该粉末一定是一种碱 D. 该粉末中一定只含有碳酸根离子
【答案】B
【解析】
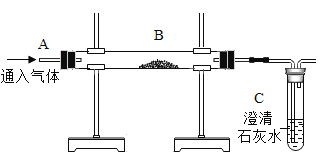
无色溶液加入酚酞变红,该溶液显碱性,加酸产生无色无味的气体,且该气体能使澄清的石灰水变浑浊,则气体为二氧化碳。
A、根据流程图可知,白色粉末溶于水,形成无色溶液,碳酸钙不溶于水,该粉末一定不是碳酸钙,故A错误;
B、碳酸钠和碳酸氢钠的溶液都是碱性的,都可以使酚酞变红,并且都能够和盐酸反应生成二氧化碳气体,故B正确;
C、碱的溶液虽然可以使酚酞变红,但能使酚酞变红的不一定碱,有的盐溶液呈碱性,同样能使酚酞变红,碱与盐酸反应没有二氧化碳生成,故C错误;
D、含有碳酸根离子和碳酸氢根离子的盐溶液,可以呈碱性;碳酸根离子和碳酸氢根离子可以与氢离子结合生成二氧化碳气体,能够产生实验中的现象,故可能含有这两种离子,故D错误。故选B。

 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案【题目】化学兴趣小组为测定一批石灰石样品中碳酸钙的质量分数,取用20 g石灰石样品,进行高温煅烧(样品除碳酸钙外,其余成分高温不分解。碳酸钙高温分解的化学方程式为CaCO3![]()
![]() CaO+CO2↑),测得石灰石煅烧过程中的不同时段剩余固体质量如下表所示:
CaO+CO2↑),测得石灰石煅烧过程中的不同时段剩余固体质量如下表所示:
煅烧的时间(min) | 剩余固体的质量(g) |
2 | 17.8 |
4 | 13.4 |
6 | 12.3 |
8 | 12.3 |
(1)完全反应后生成二氧化碳的质量______g。
(2)求石灰石样品中碳酸钙的质量分数______。
【题目】元素周期律是学习和研究化学的重要工具。下表是元素周期表的部分信息:
1H 氢 | 2He 氦 | |||||||
3Li 锂 | 4Be 铍 | 5B 硼 | 6C 碳 | 7N 氮 | 8O 氧 | 9F 氟 | 10Ne 氖 | |
llNa 钠 | 12Mg 镁 | 13A1 铝 | 14Si 硅 | 15P 磷 | 16S 硫 | 17C1 氯 | 18Ar 氩 | |
19K 钾 | 20Ca 钙 | …… | ||||||
认真分析信息,回答:
(1)地壳中含量最多的非金属元素的符号是______。
(2)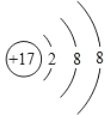 表示的是(填符号)__________;
表示的是(填符号)__________;
(3)请画出13号元素原子结构示意图________,属于_______元素(填“金属”或“非金属”),该元素在化学反应中比较容易_______(填“得到”或“失去”)电子变成____(填“阴”或“阳”)离子。