题目内容
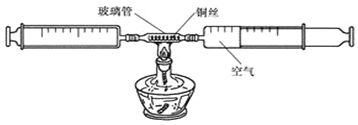
【题目】用图装置完成以下两个实验:
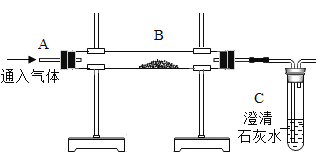
(1)探究燃烧条件:若B处盛放木炭。
Ⅰ.先在A处通入氮气一段时间后,在B处加热,B、C处没有明显变化;
Ⅱ.待B处冷却至室温,在A处通入氧气一段时间后,B、C处没有明显变化;
Ⅲ.在A处继续通入氧气,然后在B处加热,发现木炭燃烧,C处变浑浊。
Ⅰ与Ⅲ对比,说明燃烧的条件之一是_____;Ⅱ与Ⅲ对比,说明燃烧的条件之一是______;
(2)模拟工业炼铁:若B处盛放氧化铜粉末。
在A处通入一氧化碳一段时间后,B处下方用喷灯加热,
B处可观察到的现象为____________________________,
C处反应的化学方程式为__________________________,
尾气处理的方法为________________________________。
【答案】需要氧气或空气 温度要达到可燃物的着火点 固体由黑色变为红色 Ca(OH)2+CO2═CaCO3↓+H2O 在导气管的末端放一燃着的酒精灯(或用气球收集)
【解析】
(1)根据实验的过程和现象分析燃烧的条件;
(2)根据一氧化碳在高温条件下能还原氧化铁生成了铁和二氧化碳,分析实验的现象,二氧化碳能与氢氧化钙反应生成了碳酸钙和水,写出反应的化学方程式;根据一氧化碳具有可燃性分析处理尾气的方法。
(1)由实验的过程和现象可知,Ⅰ与Ⅲ对比,通入氮气不燃烧在通入氧气后能燃烧,说明燃烧的条件之一是需要氧气或空气;Ⅱ与Ⅲ对比,说明燃烧的条件之一是温度要达到可燃物的着火点;
(2)在A处通入一氧化碳一段时间后,B处下方用喷灯加热,在高温条件下,一氧化碳还原氧化铁生成了铁和二氧化碳,所以,B处可观察到的现象为:固体由红色变为黑色;由于二氧化碳能与氢氧化钙反应了碳酸钙和水,所以C处反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O,由于尾气中含有一氧化碳能污染空气,一氧化碳又具有可燃性,所以尾气处理的方法为:在导气管的末端放一燃着的酒精灯(或用气球收集)。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下表是元素周期表的一部分,则下列叙述正确的是( )
11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
A. 16号元素的离子符号是S-2
B. 氯元素的原子结构示意图是
C. 14号元素是金属元素
D. 12号元素的相对原子质量是12
【题目】如图是木炭还原氧化铜的探究实验装置
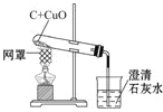
[提出问题]木炭还原氧化铜产生什么气体?
[提出猜想]产生的气体有三种情况:
①CO; ②CO2; ③________。
[设计方案]实验前后分别对试管和烧杯里
的物质进行称量,数据如下:
称量对象 | 反应前质量 | 反应后质量 | 质量差 |
试管+固体混合物 | m1 | m2 | △m1即(m1-m2) |
烧杯+澄清石灰水 | m3 | m4 | △m2即(m4-m3) |
(1)若△m2=0,说明反应产生的气体不能被澄清石灰水吸收,则猜想________成立。
(2)若猜想②正确,理论上△m1与△m2的关系是:△m1______△m2(填“>”“<”或“=”)。
[实验并记录]实验得到的数据如下表:
称量对象 | 反应前质量 | 反应后质量 | 质量差 |
试管+固体混合物 | 69.89g | 65.49g | △m1 |
烧杯+澄清石灰水 | 118.89g | 122.69g | △m2 |
用以上实验数据分析,结果应该是猜想________成立。
[反思与评价]经查阅资料知道:木炭还原氧化铜产生CO2气体,该反应的化学方程式为___。